
Glaucoma: implantes de válvula de drenaje para control de la PIO
- 22 agosto, 2019
- lightvision
- Glaucoma, Kahook Dual Blade, New World Medical, Válvula de Ahmed
El glaucoma, la segunda causa principal de ceguera en el mundo, se define como una neuropatía óptica crónica, vinculada a defectos progresivos del campo visual. En 2013, se estimó que el número total de personas de entre 40 a 80 años con glaucoma en todo el mundo era de 64.3 millones.1
Aunque se han descrito muchos factores de riesgo para el desarrollo y la progresión del glaucoma (presión intraocular [PIO], 2–5 edad, 3–5 predisposición genética, 6 y parámetros vasculares 7–9), la disminución de la PIO es el único método científicamente demostrado para retrasar la progresión de la enfermedad.
La reducción de la PIO en pacientes con glaucoma se puede lograr con terapia médica, láser o quirúrgica.10 La terapia médica es generalmente el primer paso, debido a la baja tasa de efectos secundarios. Sin embargo, cuando no se puede lograr la PIO objetivo, se debe elegir láser y / o cirugía. 11
La trabeculectomía, que fue descrita por primera vez por Cairns en 1968, 12 se considera el «estándar oro» quirúrgico para el glaucoma primario de ángulo abierto y glaucoma primario de ángulo de cierre. Las tasas de éxito de la trabeulotomía han sido variables y se han recopilado para medir la efictividad. Aunque las tasas de éxito son altas en los primeros años después de la cirugía (70% –92%), 13–15 tienden a disminuir con el tiempo (42% –90%), 16–19 especialmente en glaucomas secundarios 20–23. Además, como la trabeculectomía involucra el espacio subconjuntival anterior, está influenciada en gran medida por los procesos de curación, y la modulación de curación con antimetabolitos intraoperatorios y postoperatorios. Las derivaciones acuosas son una alternativa confiable a la trabeculectomía.24
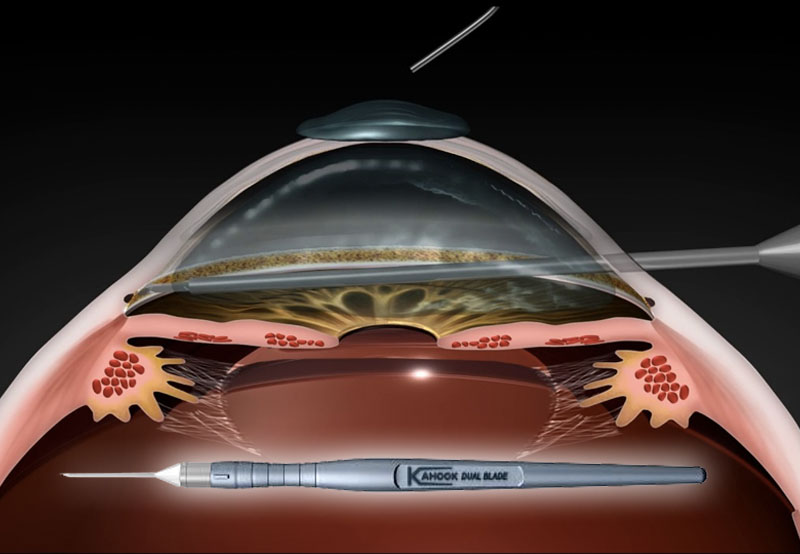
Conceptualmente, la derivación del humor acuoso (AH) al espacio subconjuntival posterior puede evitar problemas de curación, especialmente en pacientes que ya se han sometido a cirugías de glaucoma o manipulación conjuntival previa. El primer prototipo exitoso de derivación acuosa fue el implante Molteno, seguido del implante Krupin, válvula de Ahmed y Baerveldt. Mientras que en el pasado, estos dispositivos generalmente se reservaban como una cirugía de segunda opción, hoy en día la experiencia creciente ha alentado su uso también como cirugía primaria.25
VALVULA DE AHMED: descripción del dispositivo y datos técnicos
La Válvula de Ahmed proporciona un mecanismo más complejo para controlar el flujo de salida AH, que otros dispositivos. Fue desarrollado por Mateen Ahmed y aprobado por la Administración de Drogas y Alimentos en 1993. 26
Consta de 3 partes (Figura 1A): 1) una placa, en silicona de grado médico, polipropileno o polietileno poroso, según el modelo. 2) un tubo de drenaje en silicona de grado médico. 3) un mecanismo de válvula en silicona de grado médico.

El mecanismo de válvula de Ahmed consiste en membranas delgadas de elastómero de silicona, que tienen 8 mm de largo y 7 mm de ancho y crean una cámara con forma de Venturi. Las membranas están pretensadas para abrirse y cerrarse en respuesta a las variaciones de la PIO, en el rango de 8-12 mmHg.31 Después de la implantación, AH fluye lenta y continuamente hacia la cámara trapezoidal de la válvula (Figura 1B). A medida que la presión alcanza el valor umbral predeterminado, la válvula se abre, disminuyendo así la PIO. Como la sección transversal de entrada de la cámara es más ancha que la salida, se crea un diferencial de presión a través de la cámara. Este diferencial de presión permite que la válvula permanezca abierta incluso con un pequeño diferencial de presión entre la CA y los espacios subconjuntivales que rodean el dispositivo. Para que se satisfaga la ecuación de Bernoulli (fluido que fluye hacia la sección A = fluido que fluye fuera de la sección B, Figura 1B), la velocidad del fluido debe aumentar a medida que sale de la cámara a través del tubo de drenaje. Este aumento de la velocidad y el flujo no molesto explican una mejor evacuación y una menor fricción de la válvula. La tensión en las membranas de silicona ayuda a reducir la hipotonía al cerrar después de que la presión ha disminuido al nivel normal nuevamente
RESULTADOS
La implantación de la Válvula de Ahmed es un procedimiento quirúrgico eficaz y relativamente seguro, que permite manejar fenotipos particulares de glaucoma (glaucoma secundario) y glaucoma refractario a cirugías de filtración previas (cirugía de segunda elección). A pesar de una técnica aparentemente «fácil de usar», el cirujano debe adquirir muchos consejos quirúrgicos, y siempre se necesita una larga curva de aprendizaje. En comparación con otros dispositivos de drenaje de glaucoma no valvulares, la Válvula de Ahmed tiene la gran ventaja de un manejo postoperatorio más fácil. Sin embargo, la hipotonía postoperatoria temprana sigue siendo una complicación peligrosa que puede afectar este tipo de cirugía, aunque en menores casos que otros dispositivos usados.
REFERENCIAS
US NATIONAL LIBRARY OF MEDICINE NATIONAL INSTITUTES OF HEALTH https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5322839/
1. Tham YC, Li X, Wong TY, Quigley HA, Aung T, Cheng CY. Global prevalence of glaucoma and projections of glaucoma burden through 2040: a systematic review and meta-analysis. Ophthalmology. 2014;121(11):2081–2090. [PubMed] [Google Scholar]
2. Leske MC, Heijl A, Hussein M, Bengtsson B, Hyman L, Komaroff E, Early Manifest Glaucoma Trial Group Factors for glaucoma progression and the effect of treatment: the early manifest glaucoma trial. Arch Ophthalmol. 2003;121(1):48–56. [PubMed] [Google Scholar]
3. Gordon MO, Beiser JA, Brandt JD, et al. The ocular hypertension treatment study: baseline factors that predict the onset of primary open-angle glaucoma. Arch Ophthalmol. 2002;120(6):714–720. [PubMed] [Google Scholar]
4. Gordon MO, Torri V, Miglior S, et al. Ocular Hypertension Treatment Study G, European Glaucoma Prevention Study Validated prediction model for the development of primary open-angle glaucoma in individuals with ocular hypertension. Ophthalmology. 2007;114(1):10–19. [PMC free article] [PubMed] [Google Scholar]
5. Nouri-Mahdavi K, Hoffman D, Coleman AL, et al. Predictive factors for glaucomatous visual field progression in the advanced glaucoma intervention study. Ophthalmology. 2004;111(9):1627–1635.[PubMed] [Google Scholar]
6. Green CM, Kearns LS, Wu J, et al. Advanced Glaucoma Intervention Study How significant is a family history of glaucoma? Experience from the glaucoma inheritance study in Tasmania. Clin Exp Ophthalmol. 2007;35(9):793–799. [PubMed] [Google Scholar]
7. Pillunat LE, Stodtmeister R, Marquardt R, Mattern A. Ocular perfusion pressures in different types of glaucoma. Int Ophthalmol. 1989;13(1–2):37–42. [PubMed] [Google Scholar]
8. Quaranta L, Manni G, Donato F, Bucci MG. The effect of increased intraocular pressure on pulsatile ocular blood flow in low tension glaucoma. Surv Ophthalmol. 1994;(Suppl 38):S177–S181. [PubMed] [Google Scholar]
9. Quaranta L, Katsanos A, Russo A, Riva I. 24-hour intraocular pressure and ocular perfusion pressure in glaucoma. Surv Ophthalmol. 2013;58(1):26–41. [PubMed] [Google Scholar]
10. Rulli E, Biagioli E, Riva I, et al. Efficacy and safety of trabeculectomy vs nonpenetrating surgical procedures: a systematic review and meta-analysis. JAMA Ophthalmol. 2013;131(12):1573–1582.[PubMed] [Google Scholar]
11. Prum BE, Jr, Rosenberg LF, Gedde SJ, et al. Primary Open-Angle Glaucoma Preferred Practice Pattern((R)) Guidelines. Ophthalmology. 2016;123(1):P41–P111. [PubMed] [Google Scholar]
12. Cairns JE. Trabeculectomy. Preliminary report of a new method. Am J Ophthalmol. 1968;66(4):673–679. [PubMed] [Google Scholar]
13. Law SK, Shih K, Tran DH, Coleman AL, Caprioli J. Long-term outcomes of repeat vs initial trabeculectomy in open-angle glaucoma. Am J Ophthalmol. 2009;148(5):685–695.e681. [PubMed] [Google Scholar]
14. Edmunds B, Thompson JR, Salmon JF, Wormald RP. The National Survey of Trabeculectomy. II. Variations in operative technique and outcome. Eye (Lond) 2001;15(Pt 4):441–448. [PubMed] [Google Scholar]
15. Scott IU, Greenfield DS, Schiffman J, et al. Outcomes of primary trabeculectomy with the use of adjunctive mitomycin. Arch Ophthalmol. 1998;116(3):286–291. [PubMed] [Google Scholar]
16. Wilensky JT, Chen TC. Long-term results of trabeculectomy in eyes that were initially successful. Trans Am Ophthalmol Soc. 1996;94:147–159. [PMC free article] [PubMed] [Google Scholar]
17. Molteno AC, Bosma NJ, Kittelson JM. Otago glaucoma surgery outcome study: long-term results of trabeculectomy – 1976 to 1995. Ophthalmology. 1999;106(9):1742–1750. [PubMed] [Google Scholar]
18. Bevin TH, Molteno AC, Herbison P. Otago Glaucoma Surgery Outcome Study: long-term results of 841 trabeculectomies. Clin Exp Ophthalmol. 2008;36(8):731–737. [PubMed] [Google Scholar]
19. Landers J, Martin K, Sarkies N, Bourne R, Watson P. A twenty-year follow- up study of trabeculectomy: risk factors and outcomes. Ophthalmology. 2012;119(4):694–702. [PubMed] [Google Scholar]
20. Takihara Y, Inatani M, Fukushima M, Iwao K, Iwao M, Tanihara H. Trabeculectomy with mitomycin C for neovascular glaucoma: prognostic factors for surgical failure. Am J Ophthalmol. 2009;147(5):912–918.[PubMed] [Google Scholar]
21. Iwao K, Inatani M, Seto T, et al. Long-term outcomes and prognostic factors for trabeculectomy with mitomycin C in eyes with uveitic glaucoma: a retrospective cohort study. J Glaucoma. 2014;23(2):88–94.[PubMed] [Google Scholar]
22. Bettis DI, Morshedi RG, Chaya C, Goldsmith J, Crandall A, Zabriskie N. Trabeculectomy with mitomycin C or Ahmed valve implantation in eyes with uveitic glaucoma. J Glaucoma. 2015;24(8):591–599. [PubMed] [Google Scholar]
23. Singh D, Chandra A, Sihota R, Kumar S, Gupta V. Long-term success of mitomycin-augmented trabeculectomy for glaucoma after vitreoretinal surgery with silicone oil insertion: a prospective case series. Retina. 2014;34(1):123–128. [PubMed] [Google Scholar]
24. Gedde SJ, Schiffman JC, Feuer WJ, Herndon LW, Brandt JD, Budenz DL, Tube versus Trabeculectomy Study Group Treatment outcomes in the tube versus trabeculectomy (TVT) study after five years of follow-up. Am J Ophthalmol. 2012;153(5):789–803. [PMC free article] [PubMed] [Google Scholar]
25. Patel S, Pasquale LR. Glaucoma drainage devices: a review of the past, present, and future. Semin Ophthalmol. 2010;25(5–6):265–270. [PubMed] [Google Scholar]
26. Coleman AL, Hill R, Wilson MR, et al. Initial clinical experience with the Ahmed glaucoma valve implant. Am J Ophthalmol. 1995;120(1):23–31. [PubMed] [Google Scholar]
Deja un comentario cancel
Entradas recientes
- KDB GLIDE: El único dispositivo para Goniotomía aprobado por la FDA para retirar la MT y reducir la PIO.
- Goniotomía con Kahook Dual Blade versus inyección de iStent: Resultados a largo plazo en pacientes con glaucoma de ángulo abierto
- Resultados de iStent Inject versus Kahook Dual Blade en pacientes con Glaucoma sometidos a Cirugía de Cataratas
- Seguimiento a un año de un lente intraocular multifocal con optimización de la tecnología de cambio de fase elevada
- Resultados Clínicos del Implante Ahmed ClearPath en Ojos con Glaucoma: Un Novedoso Dispositivo de Drenaje sin Válvula
DIRECCIÓN
Av. Panamericana A 14 Col. Pedregal de Carrasco C.p. 04700 Coyoacán, Ciudad de México.

