
La influencia del ángulo alfa, el ángulo kappa y las aberraciones ópticas en los resultados visuales después del implante de un LIO trifocal de alta adición
- 2 marzo, 2022
- lightvision
- Cataratas, Lentes intraoculares, Liberty LIO
Guadalupe Cervantes-Coste*, André Tapia, Claudia Corredor-Ortega, Mariana Osorio, Rafael Valdez, Martha Massaro, Cecilio Velasco-Barona y Roberto Gonzalez-Salinas
Departamento de Cirugía del Segmento Anterior, Asociación para Evitar la Ceguera en México I.A.P., Ciudad de México 04030, México
Resumen: El objetivo de nuestra investigación fue examinar las posibles correlaciones entre las aberraciones ópticas, el ángulo kappa, el ángulo alfa y los resultados visuales después de una cirugía de catarata. En total, se implantó el lente intraocular (LIO) trifocal Liberty 677MY en 56 ojos de 28 pacientes. Se registraron las aberraciones de orden superior, la coma, el astigmatismo, el ángulo alfa y el ángulo kappa pre y posoperatorios, junto con la agudeza visual corregida y sin corregir a múltiples distancias. También se trazaron las curvas de desenfoque de agudeza visual y sensibilidad al contraste, y se calcularon las áreas bajo la curva a 1 y 3 meses después de la operación. Se encontraron excelentes resultados visuales en todas las distancias. Los pacientes reportaron bajos niveles de disfotopsia y el 96.4% de los pacientes se vieron totalmente libres de la necesidad de usar gafas. Mientras que el ángulo kappa disminuyó significativamente durante la cirugía de catarata (p = 0.0007), el ángulo alfa permaneció sin cambios (p = 0.5158). El ángulo alfa se correlacionó con aberraciones de orden superior (HOA) posoperatorias y tuvo un impacto negativo en la visión cercana (p = 0.0543), en tanto que la HOA y la coma corneales preoperatorias tuvieron un fuerte efecto adverso en la visión intermedia y cercana futura. Asimismo, el astigmatismo residual afectó significativamente la visión intermedia posoperatoria (p = 0.0091). Nuestros resultados sugieren que el ángulo kappa no es un factor predictivo óptimo de los resultados visuales a futuro, mientras que el ángulo alfa y la detección preoperatoria de aberraciones ópticas podrían ayudar a la selección de los pacientes antes del implante de LIOs multifocales.
Palabras clave: LIO multifocal; LIOM; ángulo kappa; ángulo alfa; aberraciones de orden superior; curva de desenfoque; resultados visuales; correlación; selección del paciente.
1. Introducción
Con el crecimiento de la demanda por un mejor estándar de vida, el interés de la gente por lograr una cómoda visión a largo plazo y estar libres de la necesidad de usar gafas ha ido en aumento [1]. Asimismo, el rápido desarrollo de las cirugías refractiva y de catarata ha hecho que la popularidad de los LIOs multifocales (LIOMs) crezca constantemente, respondiendo con éxito a estas necesidades y proporcionando una visión funcional a múltiples distancias [2,3]. Sin embargo, aunque se ha podido lograr una visión libre de gafas, los resultados posoperatorios no siempre cumplen con las expectativas preoparatorias [2,4]. Las principales causas de la falta de satisfacción reportada por los pacientes son la ametropía, la disfotopsia y la menor sensibilidad al contraste [1,5–8].
De acuerdo con lo que sabemos actualmente, no todos los pacientes se benefician de igual manera con el implante de los LIOMs, por lo que una selección cuidadosa de los pacientes y la identificación de los factores que caracterizan a «un buen candidato para recibir un LIOM» son de extrema importancia [4,9]. Además de los parámetros biométricos convencionales como la longitud axial, los valores queratométricos y la profundidad de la cámara anterior, probablemente también debería considerarse la inclusión de variables anatómicas adicionales en la evaluación preoperatoria y la planeación quirúrgica [2,7,9].
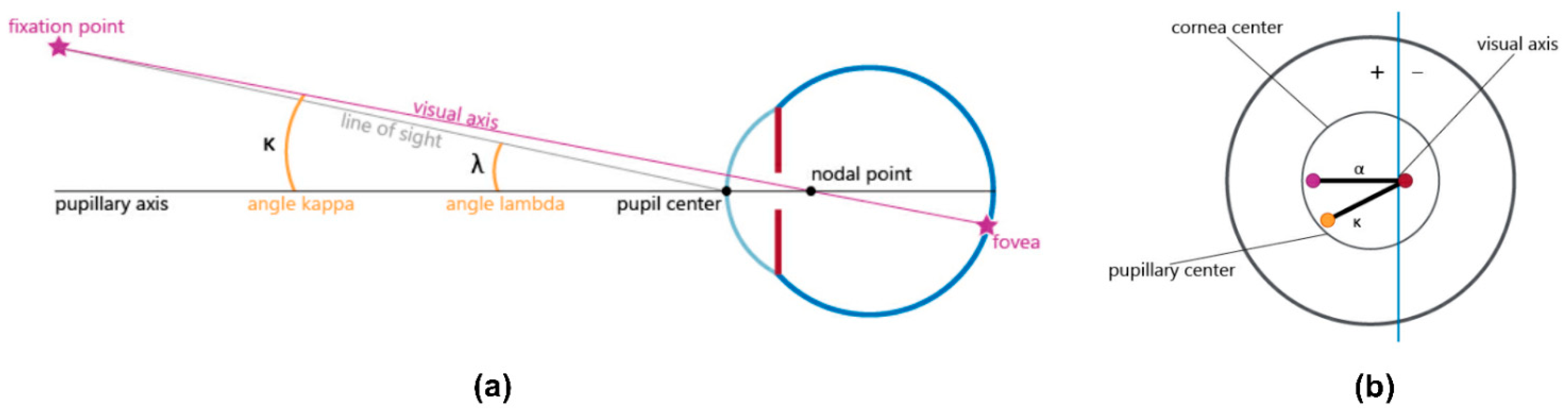
Se ha reportado con frecuencia que el tamaño de la pupila, el astigmatismo corneal y total, la coma y otras aberraciones oculares han influido en el éxito postoperatorio [2,4,10]. Además, se sabe que los LIOMs son susceptibles a mostrar cierto grado de inclinación y descentrado [11–18], lo cual afecta el funcionamiento óptico del ojo y por lo tanto reduce la calidad visual [11–18]. Esta dislocación del LIO puede estar correlacionada con el valor del ángulo kappa (la distancia angular entre los ejes visual y pupilar; Figura 1), lo que puede aumentar el riesgo de fenómenos fóticos después del implante del LIOM [11,13,19,20]. De manera similar, el ángulo alfa (la diferencia entre el eje visual y el centro del limbo) puede llevar a un pobre centrado del LIOM, lo que podría afectar el funcionamiento visual posoperatorio, además de aumentar las aberraciones de orden superior y la ametropía en el ojo pseudofáquico [7,9,21,22].
Aunque ha habido un creciente interés por demostrar el posible valor predictivo de las aberraciones ópticas, el ángulo kappa y el ángulo alfa en la selección del paciente antes del implante del LIOM, sólo se cuenta con evidencia científica limitada. Los resultados publicados a veces son contradictorios o sólo proporcionan evidencia moderadamente sólida [1,2,7,9,11– 13,19,20,23,24]. Además, la definición del ángulo kappa y el ángulo alfa no siempre es la misma en la literatura especializada y las técnicas de medición a menudo varían en los diferentes estudios [25], por lo que los resultados publicados son difíciles de comparar y resulta imposible sacar conclusiones apropiadas.
El objetivo de la presente investigación fue examinar los resultados visuales después del implante de un LIO trifocal de alta adición y probar si hay alguna correlación entre el desempeño visual alcanzado y los valores pre y posoperatorios de las aberraciones de orden superior, la coma, el ángulo kappa y el ángulo alfa.
2. Materiales y métodos
El presente estudio se realizó en conformidad con las directrices de la Declaración de Helsinki y fue aprobado por la COFEPRIS en la Ciudad de México, México (17 Cl 09 003 142; agosto de 2019).
Antes de cualquier intervención, cada paciente fue informado con detalle acerca del objetivo, el proceso y los posibles riesgos de la cirugía y de nuestra investigación clínica. Cada uno de ellos dio su consentimiento previo por escrito para participar en el estudio.
Sólo se aceptaron sujetos adultos con cataratas relacionadas con la edad en el grupo de pacientes. Ninguno de los pacientes tenía astigmatismo corneal de más de 1.5 dioptrías antes de la operación y todos ellos tenían condiciones de salud ocular normales aparte de las cataratas. Se tuvo especial cuidado de no incluir a sujetos con enfermedades oculares congénitas, trauma ocular o cirugías oculares previas, o desórdenes de la retina. Ninguno de los participantes mostró signos de inflamación ocular, glaucoma, ambliopía, inestabilidad zonular o alguna enfermedad de la córnea.
La cirugía de catarata bilateral se realizó en cada sujeto con la técnica de facoemulsificación stop-and-chop estándar bajo anestesia tópica. El intervalo promedio entre la primera cirugía y la cirugía del ojo contralateral fue de una semana. Todas las cirugías fueron realizadas por el mismo cirujano (G.C.-C.) entre marzo de 2019 y diciembre de 2020. Para todas las cirugías se emplearon incisiones principales en la córnea transparente de 2.2 mm en el meridiano vertical y una incisión secundaria de 1 mm. Se aplicó el producto viscoquirúrgico oftálmico (OVD) DiscoVisc (4% de sulfato de condritina sódica, 1.65% de hialuronato de sodio) en todas las cirugías (Alcon Laboratories, Fort Worth, TX, USA). Después de crear manualmente la capsulorrexis, el lente con catarata fue removido mediante aspiración cortical y en cada caso se implantó un LIO trifocal de acrílico hidrofílico con corrección de la presbicia con una adición intermedia de +1.75 dioptrías (D) y cercana de +3.5 D (Liberty 677MY; Medicontur Medical Engineering Ltd., Zsámbék, Hungría) en el saco capsular. La potencia esférica óptima de cada lente se seleccionó con base en el cálculo del LIO usando la fórmula de Haigis en el programa de cálculo en línea del fabricante (https://toriccalculator.net al 14 de marzo de 2019). En cada caso la refracción objetivo fue la emetropía, tomando en cuenta el astigmatismo quirúrgicamente inducido (SIA) por el cirujano. Asimismo, en cada caso las hápticas del LIO se colocaron a las 6 y 12 en punto. Después de remover el OVD restante, las heridas se cerraron con suturas de nylon 10.0.
Las mediciones preoperatorias incluyeron un examen completo de los segmentos oculares anterior y posterior, incluyendo la retina. Además de la presión intraocular (PIO), se registraron los valores queratométricos anterior y total (K1, K2), longitud axial (AXL), astigmatismo corneal y refracción subjetiva esférica y cilíndrica (SPH, CYL, respectivamente). También se midieron la agudeza visual lejana corregida y sin corregir (CDVA, UDVA) y la agudeza visual intermedia y cercana sin corregir (UIVA y UNVA, respectivamente). La pupilometría fótópica y mesópica, la determinación de las aberraciones de orden superior (HOA), astigmatismo y coma total, corneal e interna y la medición del ángulo kappa y del ángulo alfa se realizaron con el aberrómetro de frente de onda OPD-Scan III (Nidek Co., Ltd., Gamagori, Aichi, Japón). Las aberraciones refractivas se expresaron en forma de valores de raíz cuadrática media (RMS).
Las mismas mediciones se repitieron un mes después de la operación y se dio seguimiento a todos los pacientes en una visita adicional tres meses después de la cirugía. En cada caso se registraron la refracción subjetiva esférica y cilíndrica, la agudeza visual lejana corregida y sin corregir, y la agudeza visual intermedia y cercana sin corregir. También se preguntó a los pacientes si percibían algún evento disfotópico (deslumbramiento, halo, destellos, fantasmas) y, si lo hacían, la frecuencia con la que lo experimentaban (nunca, rara vez, de vez en cuando, a menudo, siempre). Asimismo, se les preguntó si tenían alguna otra dificultad relacionada con la visión. En cada caso se examinaron y registraron los posibles eventos adversos o comorbilidades oculares.
Las curvas de desenfoque monocular de agudeza visual corregida y sin corregir y de sensibilidad al contraste (VADC y CSDC, respectivamente) se midieron y trazaron uno y tres meses después del implante del LIO usando la aplicación Multifocal Lens Analyzer 3.0 diseñada para dispositivos iPad (Qvision, Madrid, España; defocuscurve.com (2 de enero de 2022)) [27]. Durante las mediciones y análisis se aplicaron las recomendaciones y protocolos proporcionadas por los desarrolladores [28]. El rango de desenfoque se midió entre +1.00 y −4.00 D con incrementos de 0.5 D en cada caso. Para cada curva de desenfoque el sistema calculó el área bajo la curva (AUC) en el rango total y en las regiones lejana, intermedia y cercana. Se usó un valor logMAR 0.3 como línea de base en los cálculos de la AUC de agudeza visual.
El conjunto completo de datos obtenidos durante el estudio está disponible al público después de su disociación en el repositorio de datos de Mendeley en doi:10.17632/w5ws4pzzxr.1 (acceso el 6 de diciembre de 2021) [29].
El análisis estadístico se realizó usando el software GraphPad Prism ver. 9.2.0 (GraphPad Software Inc., San Diego, CA, USA). Las estadísticas descriptivas (media, desviación estándar, mínimo, máximo, mediana, intervalos de confianza de 95%, etc.) se calcularon para cada variable. La normalidad de cada variable se examinó usando las pruebas de D’Agostino y Pearson. La comparación de las variables pre y posoperatorias equivalentes se hizo usando la prueba t pareada o la prueba Wilcoxon no paramétrica con base en la distribución normal de los datos. Los análisis de correlación y los análisis de regresión lineal se realizaron para revelar las posibles correlaciones entre la biometría y las características corneales pre y posoperatorias, así como los resultados visuales. La prueba rho de Spearman de correlación parcial se realizó con el software estadístico IBM SPSS Statistics 28.0 (IBM Co., Armonk, NY, USA). En cada caso un valor p <0.05 se consideró estadísticamente significativo y los datos se presentaron como media ± desviación estándar (SD).
3. Resultados
Los datos pre y posoperatorios de 56 ojos pertenecientes a 28 sujetos se incluyeron en el análisis. Las características preoperatorias de la población de pacientes se resumen en la Tabla 1. La edad promedio del grupo de estudio que incluyó a 17 mujeres (60.7%) y 11 hombres (39.3%) fue de 66.9 ± 10.1 años (min. 45; máx. 82 años).

3.1. Resultados visuales y refractivos
Tanto la refracción esférica como el equivalente esférico mejoraron significativamente después de la cirugía (Preop. vs. Mes 1: SPH: p = 0.110; SEQ: p = 0.0074; Preop vs. Mes 3: SPH: p = 0.0053; SEQ: p = 0.0142) y los resultados refractivos fueron estables durante los primeros tres meses después de la operación (SPH: p = 0.8495; SEQ: p = 0.3339) (Tabla 2).
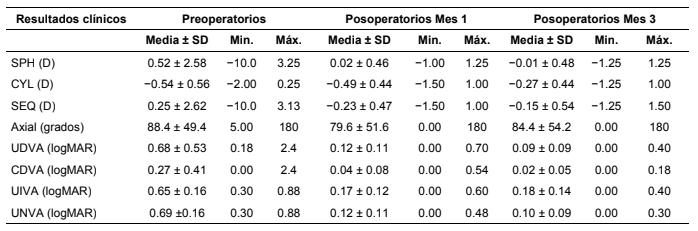
La UDVA, CDVA, así como la UIVA y UNVA mostraron una mejoría significativa (p < 0.0001 en cada caso) (Tabla 2). Los resultados visuales fueron estables, aunque la UDVA mostró una mayor mejoría entre el primero y el tercer mes después de la operación (p = 0.0076).
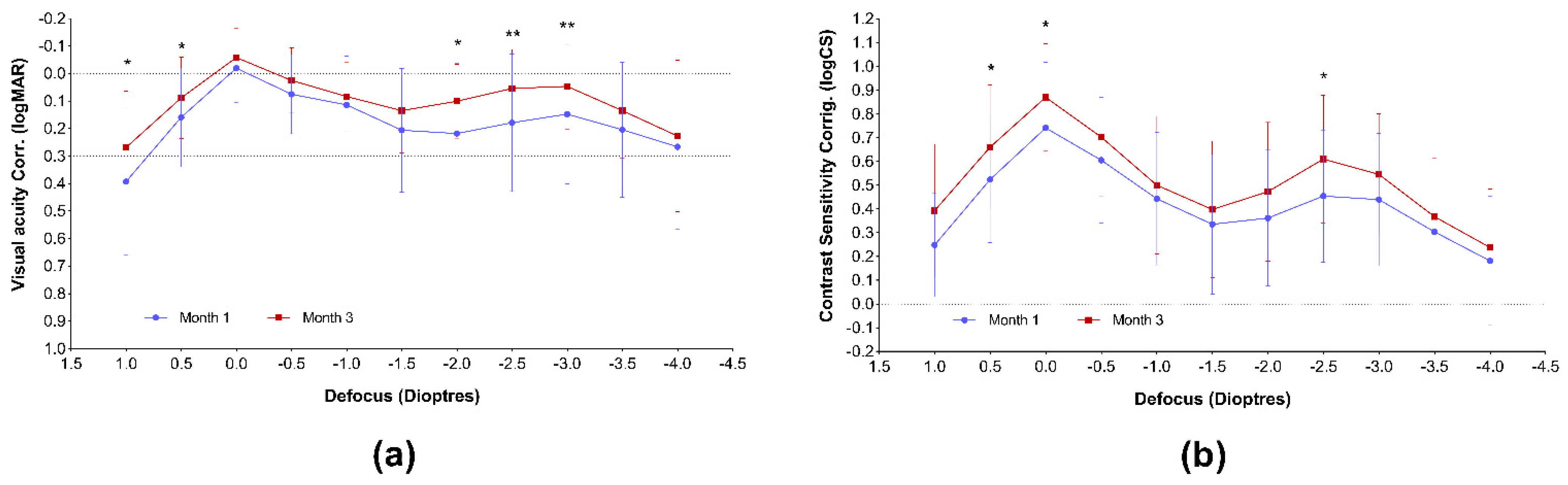
Las curvas de desenfoque de agudeza visual corregida y sensibilidad al contraste se muestran en la Figura 2. Ambas curvas representan una visión nítida a través de todo el rango de desenfoque. Las curvas obtenidas en la segunda visita posoperatoria parecen mejorar en comparación con los resultados del mes 1; sin embargo, sólo se pudo revelar una mejoría significativa entre −2.0 y −3.0 dioptrías de desenfoque (50 a 33 cm de distancia del ojo) en el caso de la agudeza visual, y sólo en el rango lejano y a −2.5 D (40 cm) en el caso de la curva de sensibilidad al contraste.
La evaluación del área bajo la curva confirmó la mejoría de la agudeza visual cercana entre el primer y tercer mes después de la operación (Tabla 3) y también demostró un área más grande en el rango total examinado.
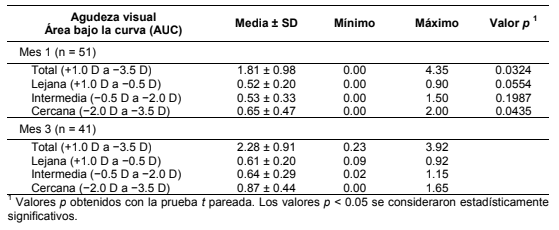
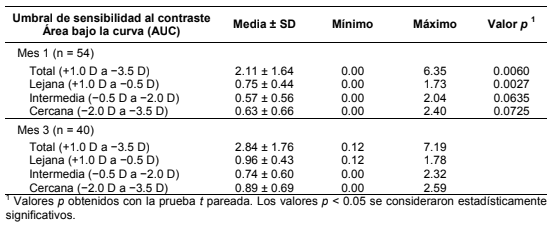
De manera similar, los cálculos de la AUC confirmaron el aumento en el rango total y lejano en el caso de la sensibilidad al contraste (Tabla 4).
3.2. Calidad visual: independencia de las gafas, disfotopsia y eventos adversos
Casi todos los 28 pacientes (96.4%) quedaron libres de la necesidad de usar gafas en todas las distancias. Sólo hubo un paciente que ocasionalmente necesitó corrección adicional en uno de los ojos.
Asimismo el descentrado del LIO se pudo observar en 2 de 56 ojos (3.57%).
La disfotopsia (halo, deslumbramiento en la noche) fue reportada por 2 de los 28 pacientes (7.14%), aunque su condición mejoró y rara vez tuvieron alguna queja al final del tercer mes después de la operación. Los mismos dos pacientes desarrollaron una opacificación de la cápsula posterior (OCP), aunque ya habían mostrado metaplasia de la cápsula posterior antes de la cirugía de catarata. La OCP también se pudo detectar en un ojo de otro paciente. También se requirió de capsulotomía con láser Nd:YAG en dos ojos de dos pacientes entre la octava y décima semanas posteriores a la operación.
3.3. Aberraciones refractivas y ángulos notables (Kappa y Alfa)
Se determinaron el astigmatismo, la coma, las aberraciones de orden superior corneal, interna y total, y los ángulos kappa y alfa antes y un mes después del implante del LIO. Los valores pre y posoperatorios equivalentes se compararon en parejas y se encontró que la coma total y las HOA internas se redujeron significativamente en comparación con los niveles preoperatorios (Tabla 5; p = 0.0259 y p = 0.0129, respectivamente). De manera similar, el ángulo kappa mostró una disminución significativa, tanto en condiciones fotópicas como mesópicas (p = 0.0007 y p < 0.0001, respectivamente). Todos los otros parámetros examinados, incluyendo el ángulo alfa, permanecieron sin cambios.

Se realizaron los análisis de correlación para revelar el posible impacto del ángulo kappa y el ángulo alfa previos a la operación en los resultados visuales futuros y en la cantidad de aberraciones de orden superior. De manera similar se evaluó la contribución potencial de las HOA y la coma preoperatorias en la agudeza visual posoperatoria. También se evaluó el impacto del astigmatismo corneal residual en los resultados visuales.
No se pudo encontrar una correlación significativa entre el valor del ángulo kappa preoperatorio y las HOA o la agudeza visual posoperatorias (Tabla 6). Por el contrario, se encontró una débil correlación entre el ángulo kappa posoperatorio y la visión intermedia no corregida después de la operación (UIVA; p = 0.0219; Tabla 6).


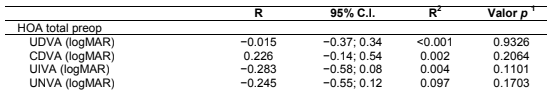
De manera similar, no se encontraron correlaciones entre el ángulo alfa preoperatorio y las HOA y agudeza visual medidas después de la cirugía (Tabla 7). Por el contrario, el ángulo alfa posoperatorio mostró tener un impacto negativo en la visión intermedia (Tabla 7; r = −0.269; R2 = 0.098; p = 0.0219). No se pudo verificar ninguna contribución significativa en la visión lejana y cercana no corregida, aunque un mayor número de casos posiblemente revelarían una correlación existente con el ángulo alfa.

También se evaluó el posible impacto de las HOA (total y corneal) y la coma (total y corneal) preoperatorias en los resultados visuales posoperatorios (Tabla 8). La HOA preoperatoria total no mostró ninguna correlación notable con la agudeza visual futura, mientras que la HOA corneal se correlacionó significativamente con la CDVA y la UIVA posoperatorias (r = 0.417; R2 = 0.264; p = 0.0126 y r= −0.459; R2 = 0.217; p = 0.0056, respectivamente). Por su parte, se encontró que la coma total preoperatoria tuvo un notable impacto negativo en la UIVA y la UNVA posoperatorias (r= −0.379; R2 = 0.042; p = 0.0296 y r= −0.433; R2 = 0.104; p = 0.0118, respectivamente), en tanto que la coma corneal preoperatoria tuvo una influencia significativa en la CDVA (r= 0.352; R2 = 0.210; p = 0.0411) y un gran impacto negativo en la UIVA (r= −0.536; R2 = 0.255; p = 0.0011).

Se encontró que el astigmatismo corneal residual tuvo el mayor impacto en la UIVA (Tabla 9; r= 0.365; R2 = 0.173; p = 0.0091), pero no se pudo encontrar ninguna correlación significativa con la UDVA, CDVA o UNVA.

4. Discusión
El implante de LIOs multifocales ofrece un método popular y eficiente para la corrección de la presbicia durante la cirugía de catarata o el cambio de lente refractivo; sin embargo, en algunos casos los resultados visuales no cumplen con las expectativas preliminares [30]. Por lo tanto, una mejor evaluación preoperatoria y la identificación de parámetros ópticos que permitan predecir los resultados quirúrgicos futuros son de gran importancia, ya que dichas medidas pueden ayudar de manera eficiente a la selección apropiada de los pacientes.
En el presente estudio investigamos las posibles correlaciones entre las aberraciones ópticas pre y posoperatorias y los resultados visuales después del implante binocular de un MIOL de alta adición.
La UDVA, UIVA, UNVA y CDVA mostraron una mejoría significativa en comparación con los valores preoperatorios (<0.0001 en cada caso). La agudeza visual medida 1 y 3 meses después de la operación fueron similares, aunque se pudo observar una ligera mejoría de la visión lejana. Esto pudo deberse a la modificación de la geometría interna del ojo después del implante del LIO [31], a los procesos de neuroadaptación [32] o a un ligero descentrado del LIO que se reportó previamente con el lente Liberty 677MY [17]. Una importante limitación del presente estudio es que no se realizaron mediciones exactas del descentrado del LIO y, por lo tanto, su contribución a los resultados visuales no pudo ser evaluada. No obstante, nuestros resultados de agudeza visual están de acuerdo con las mediciones reportadas por otros estudios después del implante del mismo LIOM [17,33].
La aplicación MLA para iPad demostró ser una herramienta rápida y fácil de usar en nuestra práctica clínica para obtener las curvas de desenfoque de agudeza visual y sensibilidad al contraste. Ambas curvas confirmaron la buena calidad de visión a lo largo de todo el rango de desenfoque, lo que se confirmó más adelante con la total independencia de las gafas lograda por la mayoría de los pacientes. Nuestras curvas de desenfoque de agudeza visual (VADC) son similares a las reportadas en estudios anteriores después del implante del mismo LIO para la corrección de la presbicia [17,28]. Encontramos importante trazar las curvas de agudeza visual además de las curvas de desenfoque de sensibilidad al contraste (CSDC), ya que estas curvas son más sensibles a los pequeños cambios en la calidad óptica [28,34]. Los estudios que evalúan las diferencias en la sensibilidad al contraste entre LIOMs con pruebas clínicas de la función de sensibilidad al contraste (CSF) normalmente miden sólo la distancia lejana y su utilidad para detectar las pequeñas diferencias en la calidad óptica entre LIOMs es cuestionable [28]. La medición de la CSDC es más bien similar a la respuesta de enfoque directo (TFR) en el banco óptico [28]. Más aún, las letras usadas en la aplicación no son comparables con las rejillas sinusoidales [28] y también hay una diferencia en la luminancia de fondo entre los dos tipos de pruebas [28]. Por lo tanto, la sensibilidad al contraste medida con la aplicación MLA es diferente de la medida normalmente con la técnica CSF convencional y la comparación de nuestros resultados con otros datos publicados podría resultar engañosa. No obstante, creemos que la CSDC es de un alto valor agregado al dar información sobre la calidad visual a través de todo el rango de visión y no sólo en la región de la distancia lejana. El curso de nuestras curvas CSDC corresponde a las reportadas por Fernández et al., quienes dieron seguimiento al implante del mismo LIOM usando la misma aplicación para iPAD [35]. Sin embargo, las AUC calculadas son difíciles de comparar con las publicadas anteriormente por el grupo español [17,28], ya que el rango de desenfoque exacto y la definición de los rangos lejano, intermedio y cercano difieren ligeramente de los usados en nuestra evaluación. Si comparamos las AUC calculadas 1 y 3 meses después de la operación, se puede observar una mejoría significativa en la agudeza visual cercana (p = 0.0435), lo que lleva asimismo a un aumento en la VA-AUC total (p = 0.0324). Las AUC de sensibilidad al contraste mostraron un notable avance en el rango lejano (p = 0.0027), lo que consecuentemente resultó en el aumento de la AUC total (p = 0.0060). Creemos que, de manera similar a los resultados convencionales de agudeza visual que teníamos, estos cambios tempranos después de la cirugía se relacionan con los cambios anatómicos en la geometría interna del ojo y los procesos de neuroadaptación [31,32], aunque se necesitan mayores investigaciones para explicar el mecanismo exacto que se encuentra detrás de esto.
Se compararon los valores equivalentes pre y posoperatorios de las aberraciones ópticas total, corneal e interna. El astigmatismo no cambió significativamente, ya que en el grupo de estudio participaron principalmente pacientes que no requerían corrección del astigmatismo. No obstante, el astigmatismo corneal residual se correlacionó positivamente con la agudeza visual intermedia posoperatoria (UIVA; p = 0.0091). Nochez et al. reportaron que el astigmatismo ocular creó una zona de visión clara entre el primer meridiano principal y el segundo meridiano principal, aumentando de esta manera los valores de profundidad de foco [36]. Por su parte, Nio et al. encontraron que las aberraciones ópticas pueden incrementar la profundidad de foco al mismo tiempo que decrece la calidad visual bajo condiciones de enfoque óptimas [37]. Por lo tanto, estas aberraciones juegan un papel esencial en el balance entre agudeza y profundidad de foco, siendo ésta última un parámetro especialmente importante en los ojos pseudofáquicos [37]. En el presente estudio pudimos confirmar los hallazgos previos de que el astigmatismo está correlacionado negativamente con la sensibilidad al contraste [38]. Estas observaciones clínicas se encuentran apoyadas por las simulaciones realizadas en un modelo de ojo anatómico con un diámetro de pupila de 3.0 mm y luz monocromática a 550 nm de longitud de onda (Figura 3; datos no publicados, cortesía de Medicontur Medical Engineering Ltd.). El astigmatismo corneal no corregido contribuye a una función de dispersión de punto más alta, una mayor dispersión de la luz y una menor calidad de imagen con LIOs monofocales (Bi-Flex 677ABY), en comparación con una situación sin ninguna aberración; pero su impacto negativo en la calidad visual es notablemente mayor en el rango intermedio del LIOM (Liberty 677MY) hecho del mismo material y con el mismo diseño.

También su pudo observar una disminución significativa en los valores de la coma total (p = 0.0259). Resultados similares fueron reportados por otros investigadores después del implante de LIOs asféricos [7,39–41]. Se cree que valores de coma mayores resultan en una disfotopsia intolerable, especialmente después del implante de LIOMs con óptica difractiva [4]. En nuestra cohorte ninguno de los pacientes se quejó de una disfotopsia severa, lo que estaría en concordancia con una coma de valores RMS bajos. De acuerdo con Santhiago et al., las aberraciones comáticas proporcionan información sobre si el LIO está centrado correctamente [8]. También se ha hipotetizado que los valores de la coma están asociados con la inclinación del LIO [12,14]. En el presente estudio no se pudo detectar ninguna inclinación del LIO en ninguno de los ojos examinados. Se observó una ligera dislocación del LIO en un caso, pero los valores de la coma posoperatorios fueron bajos (0.18), aunque ligeramente más altos que el valor preoperatorio del mismo ojo (0.10). Con base en este evento único, sería infundado sacar conclusiones. No obstante, debe hacerse notar que los valores preoperatorios de la coma total se correlacionaron negativamente con los resultados visuales intermedios y cercanos (UIVA, UNVA) futuros. Asimismo, la coma corneal parece predecir defectos en la UIVA posoperatoria, así como en la CDVA. No se encontraron datos previos en la literatura que pudieran ayudarnos a entender esta correlación. La etiología de estas interacciones deberá ser explicada mediante exámenes futuros.
Ni la HOA total ni corneal mostraron diferencias notorias entre los valores pre y posoperatorios (p = 0.0815; p = 0.7493, respectivamente). En contraste, la HOA interna mostró una disminución estadísticamente significativa en comparación con los valores preoperatorios. Resultados similares se publicaron en un artículo reciente de Lee et al. [7], aunque revelaron una disminución significativa en las HOA interna y total. Esto pudo deberse al mayor número de ojos (n = 73) incluidos en su análisis, en comparación con los 56 ojos de nuestra investigación. Por su parte, un estudio taiwanés reportó una correlación entre la HOA corneal y la CDVA posoperatoria [7]. Estos resultados fueron confirmados por la presente investigación (r = 0.417; R2 = 0.264; p = 0.0126). Además, también pudimos identificar una correlación inversa existente entre la HOA corneal preoperatoria y la UIVA. Para evitar cualquier confusión, revisamos que esta correlación no fuera un falso positivo que reflejara el posible impacto de la SEQ residual. La prueba rho de Spearman de correlación parcial (que mide la SEQ residual) confirmó que la asociación entre la HOA corneal preoperatoria y la UIVA posoperatoria era significativa (r= −0.461; p = 0.006). Como reportó Maeda [42], un leve aumento en las HOAs puede ser la causa de los resultados menos que óptimos de los LIOs multifocales. Más aún, propuso que la evaluación preoperatoria del astigmatismo corneal irregular y el consentimiento informado acerca de los efectos del mismo en la calidad de la visión serían útiles para evitar las quejas después de la cirugía incluso para los candidatos con LIOs convencionales [42].
Se ha hipotetizado que el ángulo kappa contribuye al fenómeno disfotópico posoperatorio (halo y deslumbramiento) después del implante del LIOM [1,11,19,20]. Algunos autores incluso han sugerido usar el ángulo kappa preoperatorio como una forma de predecir la calidad visual futura y han asumido que se use el ángulo kappa como un factor decisivo en la selección de los pacientes [11,19,20,24]. De acuerdo con publicaciones recientes [2] y nuestra propia investigación, esta puede haber sido una conclusión prematura. Nosotros encontramos una diferencia significativa entre los ángulos kappa pre y posoperatorios del mismo ojo, tanto en condiciones fotópicas como mesópicas (p = 0.0007 y p < 0.0001, respectivamente). Más aún, el ángulo kappa preoperatorio no mostró ninguna correlación con los valores de agudeza visual o HOA medidos después de la operación. Esto está en conformidad con los resultados recientemente obtenidos después del implante de varios LIOMs (AT LISA tri 839MP, PanOptix) [1,2]. Un ángulo kappa grande se define como aquel que excede la mitad del diámetro de la zona óptica central del LIOM [43]. De acuerdo con los resultados anteriores [44], este considerable ángulo kappa tiene mayor probabilidad de causar un descentrado del LIO, lo que posiblemente induzca disfotopsia y una disminución de la calidad visual [11,13]. Sin embargo, en la presente investigación sólo dos pacientes con opacificación de la cápsula posterior reportaron disfotopsia, aunque ambos ya habían mostrado metaplasia de la cápsula posterior antes de la cirugía de catarata. El tamaño de sus ángulos kappa no era particularmente grande y no se observó ninguna dislocación del LIO en ninguno de sus ojos. El análisis de la correlación entre el ángulo kappa y las AUC de las curvas de desenfoque de agudeza visual y sensibilidad al contraste tampoco pudo confirmar ninguna interacción (no se muestran los datos). Nuestros resultados concuerdan con los reportados anteriormente por Velasco-Barona et al. [2] y los publicados por Fernández et al., es decir, que el ángulo kappa o la cuerda mu no tuvieron ninguna relación con las AUC [18]. Esto sugiere que el ángulo kappa preoperatorio puede no ser apropiado para predecir los futuros resultados visuales. No obstante, el ángulo kappa posoperatorio mostró una correlación negativa con la UIVA (r = −0.334, R2 = 0.098, p = 0.0219), aunque la interpretación exacta y la importancia clínica de esta correlación requiere de mayor investigación.
A diferencia del ángulo kappa, el tamaño del ángulo alfa está relacionado con el limbo, el cual es constante bajo cualquier condición [9]. En nuestra investigación se confirmó que el tamaño del ángulo alfa permaneció sin cambios durante la cirugía de catarata en condiciones de iluminación tanto fotópicas como mesópicas (p = 0.5158 y p = 0.4775, respectivamente). Múltiples estudios confirman que el ángulo alfa podría dar una estimación significativa de la visión después de la operación y ser un factor predictivo de la calidad de imagen en los pacientes con LIOM [3,7,9,45]. Nuestros resultados apoyan lo anterior, es decir, que el ángulo alfa posoperatorio tiene un impacto negativo en la visión cercana (UNVA; r = −0.315, R2 = 0.113, p = 0.0543). De acuerdo con estudios anteriores, un ángulo alfa más grande puede llevar a un pobre centrado del LIO y el descentrado podría afectar el funcionamiento visual posoperatorio [7]. En contraste, Fernández et al. han reportado que un ligero descentrado de un lente trifocal de baja adición puede inclusive ser recomendable para lograr una mejor agudeza visual cercana [18]. Debido a que no medimos el descentrado exacto en nuestro estudio, esta discrepancia aún debe ser resuelta en futuras investigaciones. Más aún, nuestros datos sugieren que el ángulo alfa posoperatorio se asocia significativamente con las HOA corneal e interna (p = 0.0009 y p = 0.0291, respectivamente). Con base en estos resultados suponemos que la asociación con la HOA total también debería ser significativa (p = 0.0779) y que un mayor número de casos muy probablemente confirmaría esta suposición. De manera similar, no se pudo detectar una correlación estadísticamente significativa entre el ángulo alfa preoperatorio y las HOA posoperatorias. A pesar de este resultado y teniendo en mente que el valor del ángulo alfa es constante durante la cirugía de catarata y considerando la tendencia encontrada en nuestros análisis de correlación (HOA total p = 0.0770; HOA corneal p = 0.0643), podemos suponer que un conjunto de datos más grande podría probar una correlación existente.
Nuestra investigación tiene varias limitaciones, pues sólo contamos con 56 ojos de 28 pacientes en nuestra evaluación; sin embargo, un número más alto de casos podría haber ayudado a comprobar nuestros resultados iniciales. Además, el rango de edad de los pacientes fue grande y pudo haber afectado los resultados. No obstante, los problemas exactos alrededor de esta cuestión no estuvieron entre los propósitos de nuestra investigación. A una alta proporción de pacientes con cataratas se les diagnostica astigmatismo corneal preoperatorio [46–48], pero dado que el modelo tórico del lente de estudio (Liberty 677MTY) no estaba disponible en nuestro país durante el periodo de estudio, varios pacientes no pudieron ser incluidos en nuestra investigación. Asimismo, la pandemia de SARS-CoV−2 también obstaculizó el reclutamiento de pacientes. Debido al número limitado de sujetos participantes en la investigación, decidimos analizar los resultados de ambos ojos, aunque estos pudieran estar correlacionados y pudieran representar un posible sesgo durante la evaluación. También estamos conscientes de que la agudeza visual y la sensibilidad al contraste son parámetros subjetivos de la visión humana y que la percepción visual es el resultado combinado del sistema óptico del ojo y los mecanismos neurales del cortex visual. Aunque nuestros resultados sugieren que algunas aberraciones ópticas contribuyen a los resultados visuales finales, la correlación exacta sólo podrá evaluarse con una evaluación objetiva de la calidad de la imagen retinal. El cociente de Strehl, el corte de la función de transferencia modular (MTF) y el índice de dispersión objetiva (OSI) no se registraron durante nuestra investigación. Sin embargo, no debe ignorarse el hecho de que la actividad cerebral con frecuencia es capaz de corregir cualquier posible defecto de las imágenes retinales derivadas de aberraciones ópticas [49]. A pesar de este hecho, desde una perspectiva clínica el principal objetivo del cirujano es restaurar la visión subjetiva del paciente y, por lo tanto, la identificación de formas capaces de predecir los resultados visuales futuros definidos mediante parámetros subjetivos antes de una operación puede ser aceptable y justificada.
5. Conclusiones
Con base en nuestros resultados, el ángulo kappa no parece ser una herramienta confiable para la selección de pacientes antes del implante del MIOL, debido particularmente a que se puede esperar una disminución significativa del mismo durante la cirugía. No obstante, parece que el ángulo alfa, que se mantiene prácticamente sin cambios durante la inserción del LIO, tiene un mayor impacto en los resultados visuales futuros, definidos en términos de agudeza visual y aberraciones ópticas. Asimismo, es posible que aberraciones ópticas preoperatorias como la coma y las HOA también influyan en los resultados visuales futuros, especialmente en los rangos cercano e intermedio. Sin embargo, se necesitan más análisis con un mayor número de casos y una interpretación adecuada para obtener una comprensión más profunda de la cuestión tratada en el presente estudio.
Para ver el artículo original haz click aquí
Contribución de los autores: Concepto, G.C.-C.; metodología, R.G.-S.; software, A.T.; validación, G.C.-C. y C.C.-O.; análisis formal, R.G.-S.; recursos, M.O.; curación de los datos, R.V.; redacción—preparación del borrador original, A.T. y M.M.; redacción—revisión y edición, C.C.-O.; visualización, G.C.-C. y A.T.; supervisión, G.C.-C.; administración del proyecto, C.V.-B.; obtención del financiamiento, G.C.-C. Todos los autores han leído y están de acuerdo con la versión publicada del manuscrito.
Financiamiento: Esta investigación fue apoyada por Medicontur Medical Engineering Ltd., que proporcionó de forma gratuita los LIOMs para la investigación.
Declaración del Consejo de Revisión Institucional: Este estudio se realizó de acuerdo con las directrices de la Declaración de Helsinki y fue aprobado por la COFEPRIS en la Ciudad de México, México (17 Cl 09 003 142; agosto de 2019).
Declaración de consentimiento informado: Se obtuvo el consentimiento informado de todos los sujetos que participaron en el estudio.
Declaración de disponibilidad de los datos: El conjunto completo de datos obtenidos durante el estudio está disponible al público después de su desidentificación en el repositorio de datos de Mendeley en doi:10.17632/w5ws4pzzxr.1 [29].
Conflictos de interés: Los autores declaran que no existen conflictos de interés.
Referencias
1. Qi, Y.; Lin, J.; Leng, L.; Zhao, G.; Wang, Q.; Li, C.; Hu, L. Role of angle κ in visual quality in patients with a trifocal diffractive intraocular lens. J. Cataract. Refract. Surg. 2018, 8, 949–954. https://doi.org/10.1016/j.jcrs.2018.05.026.
2. Velasco-Barona, C.; Corredor-Ortega, C.; Avendaño-Domínguez, A.; Cervantes-Coste, G.; Cantú-Treviño, M.P.; Gonzalez- Salinas, R. Impact of correlation of angle α with ocular biometry variables. J. Cataract. Refract. Surg. 2021, 10, 1279–1284. https://doi.org/10.1097/j.jcrs.0000000000000612.
3. Grzybowski, A.; Eppig, T. Angle alpha as predictor for improving patient satisfaction with multifocal intraocular lenses? Graefes Arch. Clin. Exp. Ophthalmol. 2021, 3, 563–565. https://doi.org/10.1007/s00417-020-05053-4.
4. Braga-Mele, R.; Chang, D.; Dewey, S.; Foster, G.; Henderson, B.A.; Hill, W.; Hoffman, R.; Little, B.; Mamalis, N.; Oetting, T.; et al. ASCRS Cataract. Clinical Committee. Multifocal intraocular lenses: Relative indications and contraindications for implantation. J. Cataract. Refract. Surg. 2014, 2, 313–322. https://doi.org/10.1016/j.jcrs.2013.12.011.
5. de Vries, N.E.; Webers, C.A.; Touwslager, W.R.; Bauer, N.J.; de Brabander, J.; Berendschot, T.T.; Nuijts, R.M. Dissatisfaction after implantation of multifocal intraocular lenses. J. Cataract. Refract. Surg. 2011, 5, 859–865. https://doi.org/10.1016/j.jcrs.2010.11.032.
6. Woodward, M.A.; Randleman, J.B.; Stulting, R.D. Dissatisfaction after multifocal intraocular lens implantation. J. Cataract. Refract. Surg. 2009, 6, 992–997. https://doi.org/10.1016/j.jcrs.2009.01.031.
7. Lee, C.Y.; Huang, J.Y.; Sun, C.C.; Yang, S.F.; Chen, H.C.; Lin, H.Y. Correlation and predictability of ocular aberrations and the visual outcome after quadrifocal intraocular lens implantation: A retrospective longitudinal study. BMC Ophthalmol. 2019, 1, 188. https://doi.org/10.1186/s12886-019-1195-x.
8. Santhiago, M.R.; Netto, M.V.; Barreto, J., Jr.; Gomes, B.A.F.; Schaefer, A.; Kara-Junior, N. A contralateral eye study comparing apodized diffrative and full diffrative lenses: Wavefront analysis and distance and near uncorrected visual acuity. Clinics 2009, 10, 953–960. https://doi.org/10.1590/S1807-59322009001000004.
9. Miháltz, K.; Vécsei-Marlovits, P.V. The impact of visual axis position on the optical quality after implantation of multifocal intraocular lenses with different asphericity values. Graefe’s Arch. Clin. Exp. Ophthalmol. 2021, 3, 673–683. https://doi.org/10.1007/s00417-020-05052-5.
10. Lee, H.; Lee, K.; Ahn, J.M.; Kim, E.K.; Sgrignoli, B.; Kim, T.I. Evaluation of optical quality parameters and ocular aberrations in multifocal intraocular lens implanted eyes. Yonsei Med. J. 2014, 5, 1413–1420. https://doi.org/10.3349/ymj.2014.55.5.1413.
11. Park, C.Y.; Oh, S.Y.; Chuck, R.S. Measurement of angle kappa and centration in refractive surgery. Curr. Opin. Ophthalmol. 2012, 4, 269–275. https://doi.org/10.1097/ICU.0b013e3283543c41.
12. Harrer, A.; Hirnschall, N.; Tabernero, J.; Artal, P.; Draschl, P.; Maedel, S.; Findl, O. Variability in angle κ and its influence on higher-order aberrations in pseudophakic eyes. J. Cataract. Refract. Surg. 2017, 8, 1015–1019. https://doi.org/10.1016/j.jcrs.2017.05.028.
13. Prakash, G.; Agarwal, A.; Prakash, D.R.; Kumar, D.A.; Agarwal, A.; Jacob, S. Role of angle kappa in patient dissatisfaction with refractive-design multifocal intraocular lenses. J. Cataract. Refract. Surg. 2011, 9, 1739–1740. https://doi.org/10.1016/j.jcrs.2011.07.016.
14. Ashena, Z.; Maqsood, S.; Ahmed, S.N.; Nanavaty, M.A. Effect of Intraocular Lens Tilt and Decentration on Visual Acuity, Dysphotopsia and Wavefront Aberrations. Vision 2020, 3, 41. https://doi.org/10.3390/vision4030041.
15. Hayashi, K.; Hayashi, H.; Nakao, F.; Hayashi, F. Correlation between pupillary size and intraocular lens decentration and visual acuity of a zonal-progressive multifocal lens and a monofocal lens. Ophthalmology 2001, 11, 2011–2017. https://doi.org/10.1016/s0161-6420(01)00756-4.
16. Madrid-Costa, D.; Pérez-Vives, C.; Ruiz-Alcocer, J.; Albarrán-Diego, C.; Montés-Micó, R. Visual simulation through different intraocular lenses in patients with previous myopic corneal ablation using adaptive optics: Effect of tilt and decentration. J. Cataract. Refract. Surg. 2012, 5, 774–786. https://doi.org/10.1016/j.jcrs.2011.11.036.
17. Fernández, J.; Rodríguez-Vallejo, M.; Martínez, J.; Tauste, A.; Piñero, D.P. Biometric factors associated with the visual performance of a high addition multifocal intraocular lens. Curr. Eye Res. 2018, 8, 998–1005. https://doi.org/10.1080/02713683.2018.1478981.
18. Fernández, J.; Rodríguez-Vallejo, M.; Martínez, J.; Tauste, A.; Piñero, D.P. Patient selection to optimize near vision performance with a low-addition trifocal lens. J. Optom. 2020, 1, 50–58. https://doi.org/10.1016/j.optom.2019.06.003.
19. Tchah, H.; Nam, K.; Yoo, A. Predictive factors for photic phenomena after refractive, rotationally asymmetric, multifocal intraocular lens implantation. Int. J. Ophthalmol. 2017, 10, 241–245. https://doi.org/10.18240/ijo.2017.02.10.
20. Karhanová, M.; Marešová, K.; Pluháček, F.; Mlčák, P.; Vláčil, O.; Sín, M. Význam úhlu kappa pro centraci multifokálních nitroočních čoček (La importancia del ángulo kappa para el centrado de lentes intraoculares multifocales). Ces. Slov. Oftalmol. 2013, 2, 64– 68. (en checo)
21. Soda, M.; Yaguchi, S. Effect of decentration on the optical performance in multifocal intraocular lenses. Ophthalmologica 2012, 4, 197–204. https://doi.org/10.1159/000333820.
22. Pazo, E.E.; Richoz, O.; McNeely, R.; Millar, Z.A.; Moore, T.C.; Moore, J.E. Optimized visual outcome after asymmetrical multifocal IOL rotation. J. Refract. Surg. 2016, 7, 494–496. https://doi.org/10.3928/1081597X-20160503-01.
23. Bonaque-González, S.; Jaskulski, M.T.; Carmona-Ballester, D.; Pareja-Ríos, A.; Trujillo-Sevilla, J.M. Influence of angle Kappa on the optimal intraocular orientation of asymmetric multifocal intraocular lenses. J. Optom. 2021, 1, 78–85. https://doi.org/10.1016/j.optom.2020.07.004.
24. Fu, Y.; Kou, J.; Chen, D.; Wang, D.; Zhao, Y.; Hu, M.; Lin, X.; Dai, Q.; Li, J.; Zhao, Y.E. Influence of angle kappa and angle alpha on visual quality after implantation of multifocal intraocular lenses. J. Cataract. Refract. Surg. 2019, 9, 1258–1264. https://doi.org/10.1016/j.jcrs.2019.04.003.
25. Chang, D.H.; Waring, G.O., IV. The subject-fixated coaxially sighted corneal light reflex: A clinical marker for centration of refractive treatments and devices. Am. J. Ophthalmol. 2014, 5, 863–874. https://doi.org/10.1016/j.ajo.2014.06.028.
26. Asociación Médica Mundial. Declaración de Helsinki de la Asociación Médica Mundial: Principios éticos para las investigaciones médicas en seres humanos. JAMA 2013, 20, 2191–2194. https://doi.org/10.1001/jama.2013.281053.
27. Rodríguez-Vallejo, M.; Llorens-Quintana, C.; Furlan, W.D.; Monsoriu, J.A. Visual acuity and contrast sensitivity screening with a new iPad application. Displays 2016, 44, 15–20. https://doi.org/10.1016/j.displa.2016.06.001.
28. Fernández, J.; Rodríguez-Vallejo, M.; Tauste, A.; Albarrán, C.; Basterra, I.; Piñero, D. Fast measure of visual acuity and contrast sensitivity defocus curves with an iPad application. Open Ophthalmol. J. 2019, 1, 15–22. https://doi.org/10.2174/1874364101913010015.
29. Cervantes-Coste, G. The influence of angle alpha, angle kappa and optical aberrations on the visual outcomes after implantation of a high-addition trifocal IOL_2021. Mendeley Data 2021. https://doi.org/10.17632/w5ws4pzzxr.1.
30. Holzer, M.P.; Rabsilber, T.M.; Auffarth, G.U. Presbyopiekorrektur mittels Intraokularlinsen. (Corrección de la presbicia usando lentes intraoculares). Ophthalmologe 2006, 8, 661–666. https://doi.org/10.1007/s00347-006-1382-z. (en alemán)
31. Modesti, M.; Pasqualitto, G.; Appolloni, R.; Pecorella, I.; Sourdille, P. Preoperative and postoperative size and movements of the lens capsular bag: Ultrasound biomicroscopy analysis. J. Cataract. Refract. Surg. 2011, 10, 1775–1784. https://doi.org/10.1016/j.jcrs.2011.04.035.
32. Zhang, L.; Lin, D.; Wang, Y.; Chen, W.; Xiao, W.; Xiang, Y.; Zhu, Y.; Chen, C.; Dong, X.; Liu, Y.; et al. Comparison of Visual Neuroadaptations after Multifocal and Monofocal Intraocular Lens Implantation. Front. Neurosci. 2021, 15, 719. https://doi.org/10.3389/fnins.2021.648863.
33. García-Bella, J.; Ventura-Abreu, N.; Morales-Fernández, L.; Talavero-González, P.; Carballo-Álvarez, J.; Sanz-Fernández, J.C.; Vázquez-Moliní, J.M.; Martínez-de-la-Casa, J.M. Visual outcomes after progressive apodized diffractive intraocular lens implantation. Eur. J. Ophthalmol. 2018, 3, 282–286. https://doi.org/10.5301/ejo.5001030.
34. Rodríguez-Vallejo, M.; Remón, L.; Monsoriu, J.A.; Furlan, W.D. Designing a new test for contrast sensitivity function measurement with iPad. J. Optom. 2015, 2, 101–108. https://doi.org/10.1016/j.optom.2014.06.003.
35. Fernández, J.; García-Montesinos, J.; Martínez, J.; Piñero, D.P.; Rodríguez-Vallejo, M. Posterior capsular opacification evaluation through contrast sensitivity defocus curves with two multifocal intraocular lenses of similar material. Graefes Arch. Clin. Exp. Ophthalmol. 2021, 10, 2995–3002. https://doi.org/10.1007/s00417-021-05262-5.
36. Nochez, Y.; Majzoub, S.; Pisella, P.J. Effect of interaction of macroaberrations and scattered light on objective quality of vision in pseudophakic eyes with aspheric monofocal intraocular lenses. J. Cataract. Refract. Surg. 2012, 4, 633–640. https://doi.org/10.1016/j.jcrs.2011.11.030.
37. Nio, Y.K.; Jansonius, N.M.; Fidler, V.; Geraghty, E.; Norrby, S.; Kooijman, A.C. Spherical and irregular aberrations are important for the optimal performance of the human eye. Ophthalmic Physiol. Opt. 2002, 2, 103–112. https://doi.org/10.1046/j.1475- 1313.2002.00019.x.
38. Ravalico, G.; Parentin, F.; Baccara, F. Effect of astigmatism on multifocal intraocular lenses. J Cataract Refract Surg. 1999, 6, 804– 807. doi: 10.1016/s0886-3350(99)00029-2.
39. Pérez-Merino, P.; Marcos, S. Effect of intraocular lens decentration on image quality tested in a custom model eye. J. Cataract. Refract. Surg. 2018, 7, 889–896. https://doi.org/10.1016/j.jcrs.2018.02.025.
40. Nanavaty, M.A.; Spalton, D.J.; Gala, K.B. Fellow-eye comparison of 2 aspheric microincision intraocular lenses and effect of asphericity on visual performance. J. Cataract. Refract. Surg. 2012, 4, 625–632. https://doi.org/10.1016/j.jcrs.2011.10.039.
41. Rocha, K.M.; Soriano, E.S.; Chalita, M.R.; Yamada, A.C.; Bottós, K.; Bottós, J.; Morimoto, L.; Nosé, W. Wavefront analysis and contrast sensitivity of aspheric and spherical intraocular lenses: A randomized prospective study. Am. J. Ophthalmol. 2006, 5, 750–756. https://doi.org/10.1016/j.ajo.2006.06.031.
42. Maeda, N. Assessment of corneal optical quality for premium IOLs with Pentacam. Highlights Ophthalmol. 2011, 4, 16–20. https://doi.org/10.5005/hoo-10101-39405.
43. Alió, J.L.; Pikkel, J. Multifocal Intraocular Lenses: The Art and the Practice; Springer Nature: Basingstoke, UK, 2019; p. 23.
44. Artal, P.; Berrio, E.; Guirao, A.; Piers, P. Contribution of the cornea and internal surfaces to the change of ocular aberrations with age. J. Opt. Soc. Am. A 2002, 1, 137–143. https://doi.org/10.1364/josaa.19.000137.
45. Wang, R.; Long, T.; Gu, X.; Ma, T. Changes in angle kappa and angle alpha before and after Cataract. surgery. J. Cataract. Refract. Surg. 2020, 3, 365–371. https://doi.org/10.1097/j.jcrs.0000000000000063.
46. Day, A.C.; Dhariwal, M.; Keith, M.S.; Ender, F.; Perez Vives, C.; Miglio, C.; Zou, L.; Anderson, D.F. Distribution of preoperative and postoperative astigmatism in a large population of patients undergoing Cataract. surgery in the UK. Br. J. Ophthalmol. 2019, 7, 993–1000. https://doi.org/10.1136/bjophthalmol-2018-312025.
47. Michelitsch, M.; Ardjomand, N.; Vidic, B.; Wedrich, A.; Steinwender, G. Prävalenz und Altersabhängigkeit von kornealem Astigmatismus bei Patienten vor. (Prevalencia y cambios del astigmatismo corneal relacionados con la edad en pacientes antes de la cirugía de catarata). Ophthalmologe 2017, 3, 247–251. https://doi.org/10.1007/s00347-016-0323-8. (en alemán)
48. Pang, Y.L.; Yuan, L.; Cao, X.G.; Hou, X.R.; Bao, Y.Z. Characteristics and analysis of corneal astigmatism in age-related Cataract. patients over 50 years old (Características y análisis del astigmatismo corneal en la catarata relacionada con la edad en pacientes de más de 50 años de edad). Chin. J. Ophthalmol. 2020, 5, 349–355. https://doi.org/10.3760/cma.j.cn112142-20190618-00323. (en chino)
49. Artal, P.; Chen, L.; Fernández, E.J.; Singer, B.; Manzanera, S.; Williams, D.R. Neural compensation for the eye’s optical aberrations. J. Vis. 2004, 4, 281–287. https://doi.org/10.1167/4.4.4.
Deja un comentario cancel
Entradas recientes
- KDB GLIDE: El único dispositivo para Goniotomía aprobado por la FDA para retirar la MT y reducir la PIO.
- Goniotomía con Kahook Dual Blade versus inyección de iStent: Resultados a largo plazo en pacientes con glaucoma de ángulo abierto
- Resultados de iStent Inject versus Kahook Dual Blade en pacientes con Glaucoma sometidos a Cirugía de Cataratas
- Seguimiento a un año de un lente intraocular multifocal con optimización de la tecnología de cambio de fase elevada
- Resultados Clínicos del Implante Ahmed ClearPath en Ojos con Glaucoma: Un Novedoso Dispositivo de Drenaje sin Válvula
DIRECCIÓN
Av. Panamericana A 14 Col. Pedregal de Carrasco C.p. 04700 Coyoacán, Ciudad de México.


Pingback: ciprol
Your article helped me a lot, is there any more related content? Thanks!
Your article helped me a lot, is there any more related content? Thanks!