
Primeros resultados después del implante de lentes intraoculares trifocales hidrofílicos e hidrofóbicos: desempeño visual y óptico
- 1 junio, 2022
- lightvision
- Cataratas, Lentes intraoculares, Liberty LIO, Medicontur, oftalmología
Francisco Poyales,1 Ricardo Pérez,1 Israel López-Brea,1 Ying Zhouà,1 y Nuria Garzónà1,2 1 Miranza IOA Madrid, c/Galileo 104, Madrid, España
2 Departamento de Optometría y Visión, Universidad Complutense de Madrid, c/Arcos de Jalón 118, Madrid, España
La correspondencia deberá dirigirse a Nuria Garzón en: nugarzon@opt.ucm.es
Recibido el 2 de mayo de 2021; aceptado el 22 de noviembre de 2021; publicado el 18 de diciembre de 2021
Editor académico: Nilufer Yesilirmak
Copyright © 2021 Francisco Poyales et al. Este es un artículo de acceso gratuito que se distribuye bajo los términos y condiciones de la licencia de bienes comunes creativos de Creative Commons, la cual permite su uso, distribución y reproducción ilimitadas por cualquier medio, a condición de que el trabajo original sea citado apropiadamente.
Propósito. Comparar el desempeño visual y óptico después de la cirugía de cataratas entre dos lentes intraoculares (LIOs) trifocales con el mismo diseño óptico: un LIO de acrílico hidrofóbico libre de resplandores y un LIO de acrílico hidrofílico. Método. A los pacientes se le implantó bilateralmente el LIO hidrofóbico o el LIO hidrofílico y se evaluaron los datos de los ojos derechos de los pacientes. La evaluación de la calidad visual incluyó los resultados refractivos, la agudeza visual (AV) monocular a distancias lejana, intermedia y cercana, la curva de desenfoque, las aberraciones (aberración esférica o SA, por sus siglas en inglés), la raíz cuadrática media (RMS, por sus siglas en inglés) de las aberraciones de orden superior (HOA, por sus siglas en inglés) corneal, interna y total, y la inclinación del LIO. Resultados. Se incluyeron cincuenta y un pacientes en el análisis: a 26 pacientes se les implantó el LIO hidrofóbico y a 25 pacientes se les implantó el LIO hidrofílico. No se encontraron diferencias estadísticamente significativas a 1 mes en la AV monocular lejana corregida y sin corregir, la AV intermedia y cercana con corrección lejana, la curva de desenfoque, el equivalente esférico manifiesto, la SA total y la RMS de la HOA total, interna y corneal. La curva de desenfoque de ambos grupos mostró una agudeza visual de 0.3 logMAR o mejor en el rango intermedio de 0.5 a -2.5 D de nivel de vergencia sin diferencias significativas entre los grupos. En comparación con el grupo hidrofílico, la inclinación en la dirección de las y fue significativamente más alto en el grupo con lente hidrofóbico (p = 0.027). La inclinación total y la inclinación en el eje de las x no difirió entre los grupos. Conclusión. Ambos LIOs demostraron una excelente calidad de visión y le proporcionaron al paciente un amplio rango de visión.
1. Introducción
Los lentes intraoculares (LIOs) monofocales ofrecen una excelente agudeza visual (AV), pero como sugiere el nombre, a una sola distancia—normalmente lejana. Debido a que los pacientes ya no pueden ajustar el rango de visión después del implante del LIO, necesitan usar gafas para enfocar otras distancias. La primera generación de LIOs «bifocales» proporcionó dos puntos de enfoque, uno para la visión lejana y otro para la visión cercana, pero debido al aumento en los últimos años en el uso de la computadora, las tablets y los teléfonos inteligentes, ha habido un aumento en la demanda de LIOs que también ofrezcan una buena visión intermedia—algo que no se puede lograr con los LIOs bifocales[1]. En 2010 se introdujo el primer LIO trifocal (FineVision Micro F, PhysIOL, Lieja, Bélgica) [2] y numerosos estudios han mostrado que estos LIOs proporcionan una buena agudeza visual (AV) lejana, intermedia y cercana, dando por resultado un alto grado de satisfacción de los pacientes [3–8].
El presente estudio utilizó dos LIOs trifocales PhysIOL, ambos basados en el diseño óptico del LIO FineVision Micro F, aunque diferentes en el material con que están hechos, lo que da por resultado diferencias significativas en el grosor de los LIOs. El LIO POD F GF está hecho de un material acrílico hidrofóbico libre de resplandores, el cual debería superar las conocidas desventajas de los materiales acrílicos convencionales, tanto hidrofóbicos [9] como hidrofílicos [10,11].
Este estudio compara el LIO POD F GF hidrofóbico libre de resplandores con el LIO POD F hidrofílico en términos de calidad óptica después de su implante en pacientes con cataratas.
2. Materiales y métodos
Este estudio clínico prospectivo aleatorio y controlado se realizó para comparar la calidad de visión, incluyendo la AV monocular a una distancia lejana, intermedia y cercana, los resultados refractivos, la curva de desenfoque, las aberraciones y la inclinación del LIO, en pacientes que se sometieron a una cirugía.
de catarata y al implante bilateral del LIO trifocal FineVision POD F GF o FineVision POD F. El modelo de LIO usado en el implante se eligió aleatoriamente para cada paciente.
Las pruebas clínicas (NCT03347981) siguieron los principios de la Declaración de Helsinki y fueron aprobadas por el comité local de ética (CEIC Hospital Clínico San Carlos, Madrid, España).
2.1. Modelos de LIO. Ambos modelos de LIOs usados en este estudio son lentes trifocales difractivos de una sola pieza que ofrecen tres puntos focales combinando dos perfiles difractivos superpuestos, uno con una potencia añadida de +1.75 D en el plano del LIO para la visión intermedia y otro con una potencia añadida de +3.50 D para la visión cercana (el punto focal lejano se crea mediante la luz no difractada). Ambos LIOs POD F GF y POD F tienen un diámetro de la óptica de 6 mm y un diámetro general de 11.4 mm, así como un borde cuadrado de 360° alrededor de la óptica con el fin de reducir al mínimo la opacificación de la cápsula posterior (OCP). La óptica asférica biconvexa de los LIOs compensa parcialmente las aberraciones esféricas positivas (SA) de la córnea. La principal diferencia entre los LIOs es el material con el que han sido fabricados. El LIO POD F GF está hecho de un acrilato hidrofóbico libre de resplandores con un índice de refracción de 1.52, mientras que el LIO POD F es un lente acrílico hidrofílico con filtro de luz azul y ultravioleta con un índice de refracción de 1.46. Otra diferencia menor entre ambos modelos de LIOs es el diseño de las hápticas del lente. Ambos LIOs cuentan con hápticas de C-loop doble con una angulación de 5°, aunque las hápticas del LIO POD F GF tienen una estructura adicional en forma de onda concebida para reducir el riesgo de adhesión entre las hápticas y el saco capsular durante el implante.
2.2. Pacientes. Para este estudio se contó con la participación de un total de 51 pacientes, divididos en dos grupos: el grupo POD F GF (n = 26) en el que se implantó bilateralmente el LIO POD F GF yelgrupoPODF(n=25)conelLIOPODF.Uncálculodel tamaño de la muestra señala que este número de sujetos por grupo fue adecuado para comparar la calidad óptica entre ambos grupos.
El objetivo de este artículo es presentar la calidad visual monocular de los pacientes, por lo que para evitar el sesgo se presentan aquí los resultados a 1 mes de los ojos derechos (OD) de los pacientes.
Los pacientes con catarata con una edad de 50 años o más se incluyeron después de someterse a una cirugía de catarata sin incidentes adversos o comorbilidades, con el deseo de ya no usar gafas después de la cirugía, expectativas realistas, disponibilidad, voluntad de participar y conocimientos suficientes para cumplir con los procedimientos del examen. Los criterios de exclusión fueron un astigmatismo irregular, un astigmatismo regular de > 1.0 D medido mediante biometría o queratometría automática o > 1.25 D si el eje vertical del cilindro estuvo entre 90° y 120° en uno o ambos ojos, un padecimiento o enfermedad crónica o aguda que pudiera aumentar el riesgo o confundir los resultados del estudio, un historial de trauma ocular o cirugía ocular previa incluyendo procedimientos refractivos, anormalidad zonular o capsular que pudiera afectar el centrado o inclinación del LIO después de la operación, anormalidad de la pupila u ojos en los que se sospechara DMAE.
2.3. Cirugía. La cirugía de catarata fue realizada por un cirujano experimentado (FP) usando un procedimiento de facoemulsificación estándar y una incisión de 2.2 mm. Todos excepto 4 pacientes recibieron un CTR en ambos ojos para aumentar la estabilidad de la colocación del LIO y evitar la miopización posoperatoria. Se usó el inyector Accujet 2.1 (Medicel, Thal, Suiza) en todos los implantes para estandarizar el astigmatismo quirúrgicamente inducido.
2.4. Métodos de evaluación. La evaluación preoperatoria incluyó la refracción manifiesta, la AV lejana corregida (CDVA), la presión intraocular y la biometría y queratometría corneal (IOLMaster 700, Carl Zeiss Meditec AG, Alemania).
Los principales resultados a 1 mes después de la operación incluyeron la refracción manifiesta, el error de predicción, la AV monocular lejana corregida y sin corregir (CDVA y UDVA), la AV intermedia con corrección lejana (DCIVA), la AV cercana con corrección lejana (DCNVA), la curva de desenfoque monocular y la aberrometría.
La agudeza visual lejana, intermedia y cercana se midió a 4 m, 70 cm y 35 cm, respectivamente, mediante las tablas del Estudio de Tratamiento Temprano de la Retinopotía Diabética (ETDRS) (Precision Vision, E.E.U.U.). La agudeza visual con corrección lejana (CDVA, DCIVA y DCNVA) se midió usando la refracción subjetiva para visión lejana.
Las curvas de desenfoque se generaron añadiendo un lente de desenfoque a la refracción mejor corregida de +2.0 D a −4.0 D en pasos de 0.5 D. Con cada lente de desenfoque la AV se probó a 4 m usando las tablas ETDRS.
El OPD-Scan III (Nidek Inc., Japón) se usó para medir los tamaños de pupila fotópica y mesópica, y para las mediciones aberrométricas incluyendo las aberraciones esféricas (SA), la raíz cuadrática media (RMS) de las aberraciones de orden superior (HOAs) total, corneal e interna, y la inclinación del LIO.
2.5. Análisis estadístico. El análisis de datos se realizó usando Microsoft Excel (versión 16.0) y el plug-in WinSTAT (versión 2012.1.0.96). Las estadísticas descriptivas se expresaron como una media (± desviación estándar (SD), mediana y rango). La prueba U de Mann–Whitney se usó para evaluar la importancia de las diferencias entre grupos. También se realizó la prueba de suma de rangos de Wilcoxon para datos pareados con el fin de evaluar la importancia de las diferencias entre exámenes. Un valor p de menos de 0.05 se consideró estadísticamente significativo. El error de predicción refractiva se definió como la diferencia entre el SE manifiesto posoperatorio alcanzado y el SE previsto.
El tamaño de la muestra se determinó usando la calculadora de potencia en sobre sellado. Para no mostrar ninguna diferencia entre las dos cohortes del estudio y con un abandono de 15%, el cálculo del tamaño de la muestra dio por resultado 25 pacientes por grupo de estudio.
3. Resultados
Cincuenta y uno ojos derechos se incluyeron en el análisis del estudio: 26 ojos en el grupo POD F GF y 25 ojos en el grupo POD F. Todos los pacientes tuvieron una cirugía de catarata sin incidentes adversos con el implante del LIO y completaron la fase de seguimiento de 1 mes. Los datos demográficos y la potencia del LIO se resumen en la Tabla 1. No hubo diferencias significativas en la edad, género o potencia del LIO de los pacientes entre los grupos de estudio (p > 0.05).
Como se muestra en la Figura 1, el equivalente esférico refractivo manifiesto (MRSE) a 1 mes después de la operación no difiere de manera estadísticamente significativa entre los grupos (p = 0.299). El MRSE medio fue de 0.09 ± 0.47 D en el grupo POD F GF y de 0.03 ± 0.38 D en el grupo POD F después de 1 mes. En comparación con los valores preoperatorios (POD F GF: 0.66 ± 2.35 D; POD F: 0.83 ± 2.24 D), hubo una mejora numérica, aunque no estadísticamente significativa (p = 0.112 en el grupo POD F GF y p = 0.058 en el grupo POD F).
A 1 mes después de la operación ambos grupos de estudio resultaron ligeramente hipermétropes (0.11 ± 0.44 D en el grupo POD F GF y 0.07 ± 0.38 D en el grupo POD F) sin diferencias significativas entre los grupos (p = 0.418). La Figura 2 muestra la distribución del error de predicción: 86% de los ojos en el grupo POD F GF y 80% de los ojos en el grupo POD F estuvieron dentro de ± 0.5 D del MRSE objetivo.
La agudeza visual a 1 mes después de la operación se muestra en la Tabla 2. No se observaron diferencias significativas entre los grupos POD F GF y POD F.
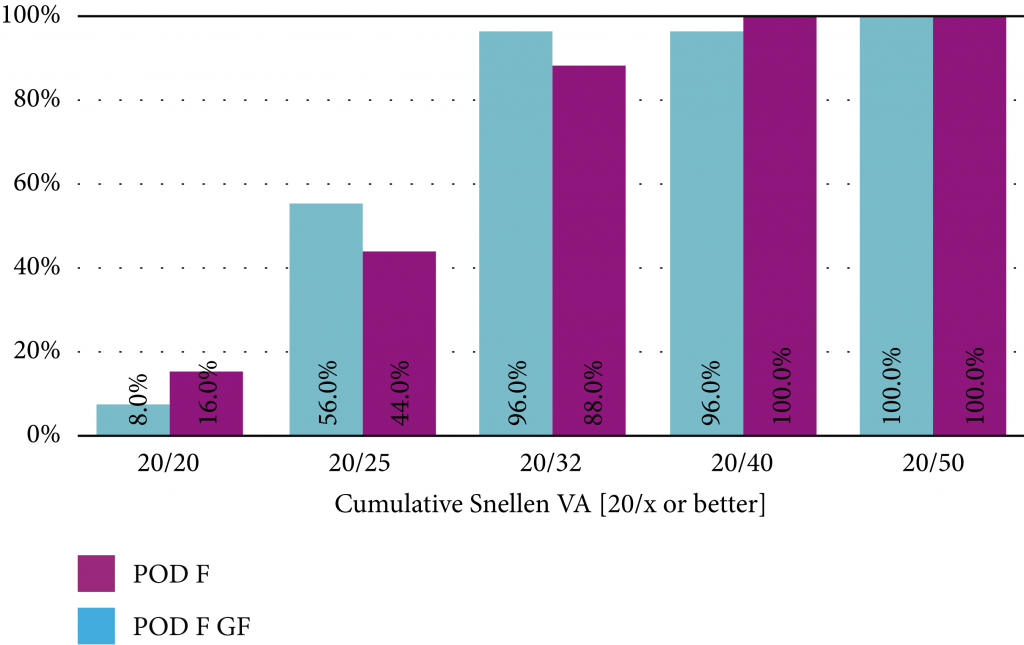
La Figura 3 muestra la distribución acumulativa de la UDVA, CDVA, DCIVA, y DCNVA para ambos grupos.
Casi el 85% de los ojos en el grupo POD F GF y 88% de los ojos en el grupo POD F tuvieron una UDVA de 20/25 o mejor y 100% de los ojos en ambos grupos tuvieron una UDVA de 20/50. La CDVA fue de 20/25 o mejor en alrededor del 96% de los ojos en el grupo POD F GF y en todos los ojos (100%) en el grupo POD F. La DCIVA y DCNVA fueron mejores a 20/40 en el 96% y 92% de los ojos en el grupo POD F GF y en todos los ojos (100%) del grupo POD F, respectivamente.
Las curvas de desenfoque monocular medio con la desviación estándar se muestran en la Figura 4.
Los máximos valores de AV se obtuvieron en ambos grupos en un nivel de vergencia de 0.0 D, correspondiente a la visión lejana. Entre las visiones lejana y cercana (es decir, niveles de desenfoque entre 0.5 y −2.5 D), todos los ojos de ambos grupos mostraron una AV de 0.3 logMAR o mejor. Los ojos que recibieron el LIO POD F tuvieron una AV significativamente mejor en los niveles de vergencia de −4.0 D, −3.5 D y −3.0 D (p = 0.013, p = 0.014 y p = 0.042) en comparación con los ojos del grupo POD F GF. Para todos los demás niveles de vergencia no hubo diferencias significativas entre ambos grupos (p > 0.05).
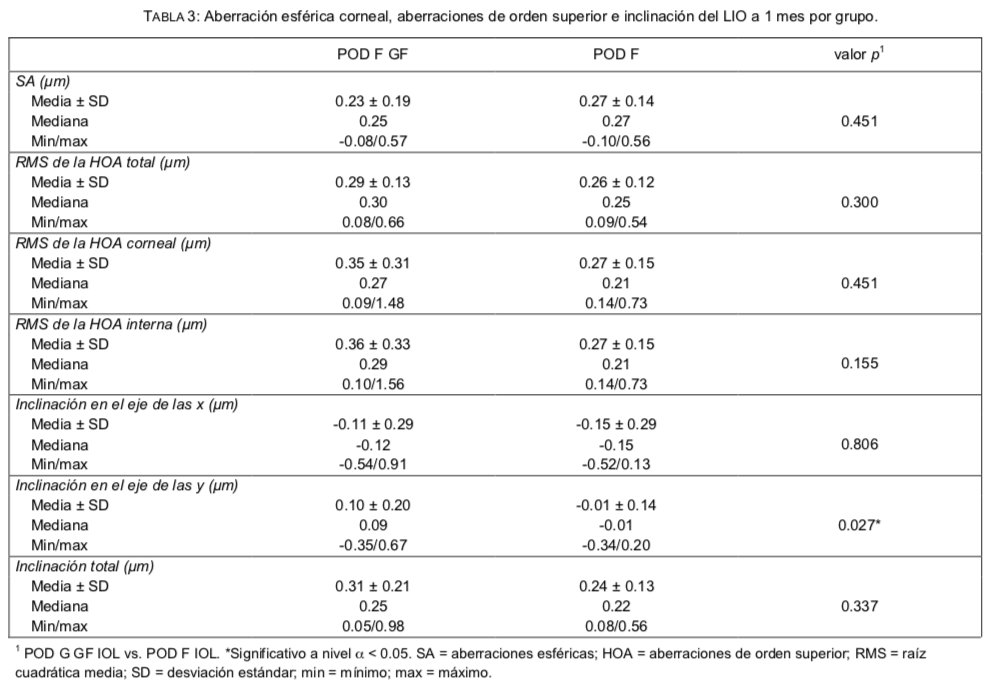
Los tamaños de pupila fotópica y mesópica no difirieron significativamente entre los grupos (p = 0.510 y p = 0.279, respectivamente). La SA, la RMS de la HOA total, interna y corneal, y la inclinación en el eje de las x, el eje de las y, y la inclinación total del lente medidas con el OPD-Scan III se muestran en la Tabla 3. La inclinación en la dirección de las y fue significativamente más alta en el grupo POD F GF que en el grupo
POD F (p = 0.027), mientras que las aberraciones esféricas, HOAs, inclinación en el eje de las x e inclinación total no difirieron entre los grupos.
En el curso de este estudio ocurrieron tres eventos adversos (AEs) y un evento adverso serio (SAE) dentro del lapso de 1 mes. Todos ellos se clasificaron como «en recuperación» después de completado el estudio.
En el transcurso del examen detallado con lámpara de hendidura después de 1 mes, un ojo del grupo POD F GF mostró una OCP «leve» (es decir, sin necesidad de tratamiento con Nd:YAG). Asimismo, en tres ojos se diagnosticó ojo seco (dos de los ojos estaban en el grupo POD F y el restante en el grupo POD F GF), y dos ojos (ambos del grupo POD F) desarrollaron uveitis (uveitis anterior y uveitis ligera, respectivamente) 1 mes después de la cirugía. En ningún caso se detectó fibrosis capsular anterior.
4. Discusión
El presente estudio clínico demostró que en los ojos en los que se implantaron el LIO POD F GF o el LIO POD F lograron una muy buena calidad de visión posoperatoria. De igual manera ambos LIOs proporcionaron una buena UDVA monocular, con el 85% del grupo POD F GF y el 88% del grupo POD F logrando una AV de 20/25 o mejor. Una DCIVA de 20/40 o mejor se logró en el 96% del grupo POD F GF y en el 100% del grupo POD F. La DCNVA fue 20/40 o mejor en el 92% del grupo POD F GF y en el 100% del grupo POD F. Los resultados de la AV lejana con el LIO POD F GF y el LIO POD F que se obtuvieron en este estudio son comparables con los de otros estudios que examinaron modelos de LIOs trifocales [5, 6, 12–16]. Con respecto a la AV intermedia y cercana, los resultados observados con LIOs trifocales en la literatura varían y van de 0.1 logMAR o mejor para la DCIVA y DCNVA [6, 12, 15, 17] a una agudeza visual muy por debajo de 0.1 logMAR [5, 17, 18]. La DCIVA y DCNVA en nuestro estudio están dentro de los rangos dados por la literatura. Sin embargo, las comparaciones directas son difíciles debido a los diferentes métodos de medición (distancias y tablas de AV) y los diferentes tamaños de las poblaciones de estudio. El desempeño en las distancias intermedia y cercana en este estudio está ligeramente por debajo del de otros estudios con los mismos LIOs o LIOs similares. Estudios con los mismos modelos o modelos similares de LIOs han mostrado que la agudeza visual intermedia mejora entre 1 y 3 meses y que la agudeza visual cercana aumenta hasta los 6 meses [12].
No hubo diferencias significativas en los resultados visuales de los ojos que recibieron los LIOs POD F GF y POD F en este estudio, por lo que concluimos que los diferentes materiales no afectan el desempeño óptico de los LIOs. No se observaron resplandores en el grupo con el POD F GF o el grupo con el POD F durante el periodo de seguimiento de 1 mes, aunque éste es un corto periodo y se requeriría un seguimiento mucho más largo para conocer el comportamiento de estos materiales a largo plazo.
Las curvas de desenfoque en los grupos POD F GF y POD F mostraron dos picos: uno en el nivel de vergencia de 0.0 D (correspondiente a la visión lejana) y uno a −2.5 D (correspondiente a 40 cm). No hubo una disminución considerable en la AV intermedia en el rango de la curva de desenfoque entre −2.5 D y 0.0 D, lo que refleja la clara ventaja que los LIOs trifocales tienen sobre los LIOs bifocales, que se asocian con una
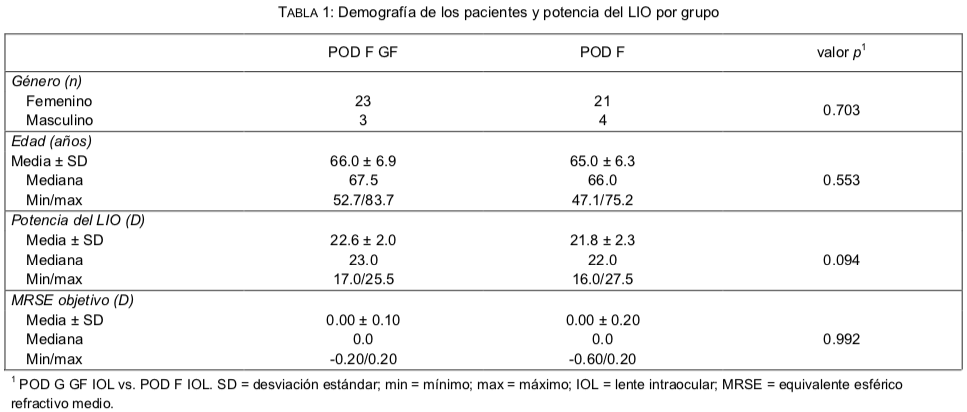
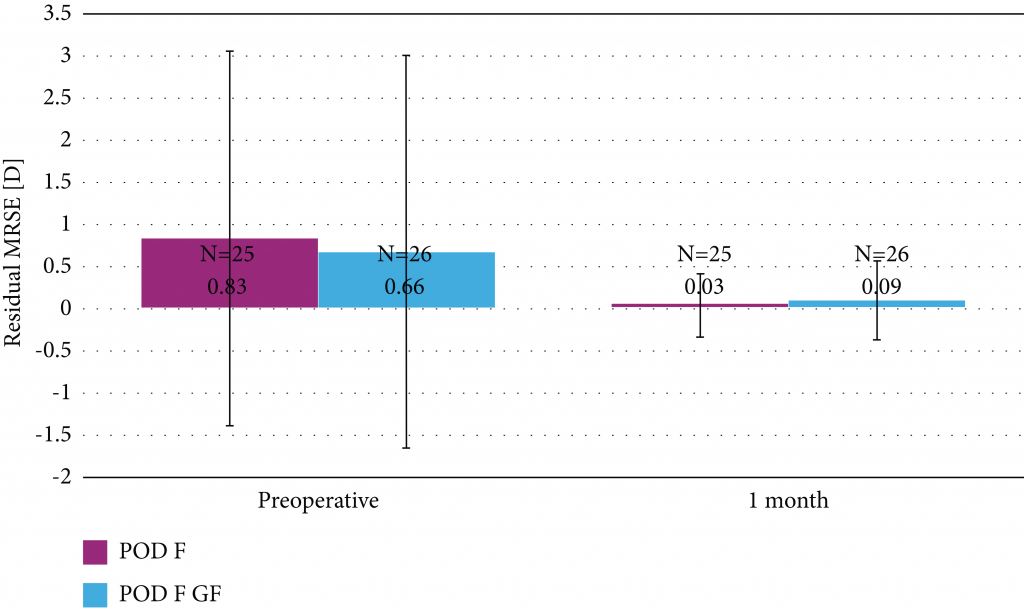
FIGURA 1: Equivalente esférico refractivo medio antes de operación y a 1 mes de operación (D).
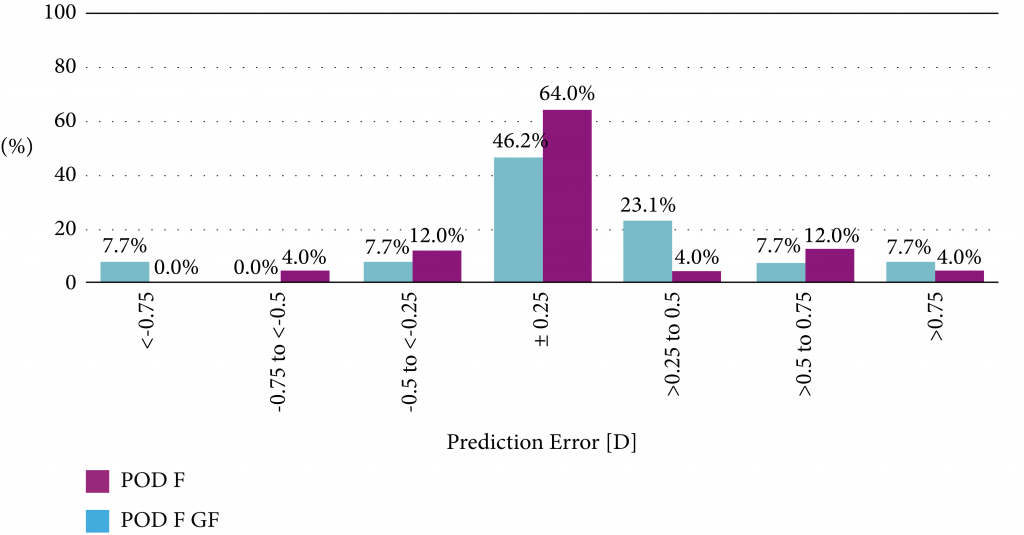
FIGURA 2: Distribución del error de predicción 1 mes después de la operación (% de ojos)
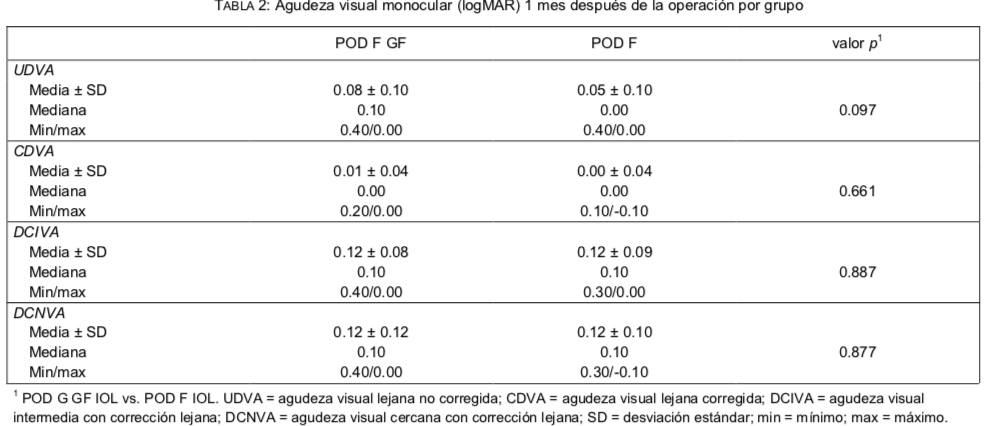
FIGURA 3: Distribución acumulativa de (a) la agudeza visual lejana no corregida (UDVA), (b) la agudeza visual lejana corregida (CDVA), (c) la agudeza visual intermedia con corrección lejana a 70 cm (DCIVA) y (d) la agudeza visual cercana con corrección lejana a 35 cm (DCNVA). La agudeza visual monocular se muestra 1 mes después de la operación para los ojos en los que se implantó un LIO POD F GF o un LIO POD F.
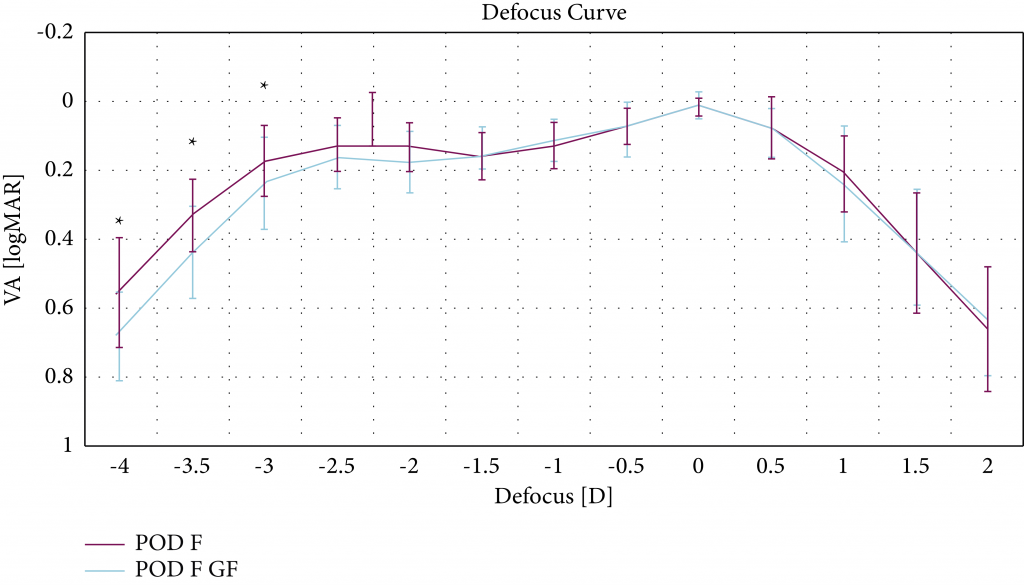
FIGURA 4: Curvas de desenfoque monocular 1 mes después de la operación para los ojos en los que se implantó un LIO POD F GF o un LIO POD F.
curva de desenfoque en forma de V, disminuyendo considerablemente en el rango intermedio entre alrededor de −0.5 Dy−1.5D[17,19–21].
En el rango intermedio ambos grupos alcanzaron valores AV entre 0.1 y 0.17 logMAR. Asimismo se observó una AV significativamente mejor en el grupo POD F a una distancia cercana entre −4.0 D y −3.0 D de desenfoque en relación con el grupo POD F GF, aunque existe la posibilidad de que esto se debiera a los tamaños de pupila (numéricamente, pero no significativamente) ligeramente más pequeños en el grupo POD F, lo que pudo haber llevado a un mejor desempeño a corta distancia [21].
La RMS de la HOA total media es un importante parámetro de medición al evaluar el desempeño óptico de un LIO, lo cual también fue comparable entre los grupos: 0.29 ± 0.13 μm en el grupo POD F GF y 0.26 ± 0.12 μm en el grupo POD F. Que las HOAs necesiten corregirse o no en la cirugía de catarata es un reto para el que todavía no se ha encontrado una respuesta definitiva, ya que la precisión requerida de centrado en estos LIOs con corrección del frente de onda es una preocupación obvia. En la mayoría de los casos, degradan la calidad de visión, aunque por el contrario también pueden tener un efecto benéfico. En el caso de la presbicia cierta cantidad de HOAs (sobre todo las SA) tienen la posibilidad de aumentar la profundidad de campo sin tener un impacto negativo en la agudeza visual. Si se retira el lente natural durante la cirugía de catarata y se reemplaza con un lente artificial, las aberraciones internas y de acuerdo con esto las aberraciones de todo el sistema óptico cambian. Ambos modelos de LIO usados en este estudio compensan parcialmente la SA positiva de la cornea proporcionando una SA de −0.11 μm en una pupila de 5 mm. Por lo tanto, los LIOs están cerca de ser «libres de aberraciones», lo que también significa una menor sensibilidad al descentrado y la inclinación, pero no necesariamente conlleva alguna desventaja en la calidad de imagen en comparación con los LIOs bifocales o con profundidad de foco extendida [22]. No se encontraron diferencias estadísticamente significativas en la SA entre los grupos de estudio.
Este estudio se enfocó en la evaluación del desempeño visual monocular después del implante de LIOs trifocales. La evaluación binocular se omitió para evitar el sesgo, pero será parte de un análisis futuro junto con un seguimiento más largo.
En el presente estudio los LIOs POD F y POD F GF mostraron muy buenos resultados visuales y una buena predictibilidad refractiva, con solo pequeñas desviaciones hacia la hipermetropía durante un periodo de seguimiento de 1 mes. Durante este corto periodo de seguimiento no se observaron desventajas asociadas con el biomaterial GF hidrofóbico del LIO POD F GF en comparación con el LIO POD F de material hidrofílico. Todas las cirugías se realizaron sin que hubiera incidentes adversos, lo que es una muestra del fácil manejo e implante de ambos modelos de LIOs.
5. Conclusión
Con base en los datos clínicos y de seguridad mostrados en este estudio, podemos concluir que el implante de ambos lentes trifocales conforme a su uso previsto parece ser una opción efectiva y segura para compensar la presbicia durante la cirugía de catarata. Sin embargo, son necesarios estudios futuros de seguimiento clínico a largo plazo y actividades de control posteriores a la comercialización para confirmar estos resultados y evaluar la independencia de las gafas y la satisfacción de los pacientes.
Disponibilidad de datos
Los autores no tienen la intención de compartir la información individual de los pacientes por una cuestión de protección de datos.
Conflictos de interés
Los autores declaran que no existen conflictos de interés relativos a la publicación de este estudio.
Reconocimientos
Este estudio fue patrocinado por PhysIOL SA, Lieja, Bélgica.
Referencias
[1] S. Jin, D. S. Friedman, K. Cao et al., “Comparison of post- operative visual performance between bifocal and trifocal intraocular Lens based on randomized controlled trails: a meta-analysis,” BMC Ophthalmology, vol.19, no. 1, p. 78, 2019.
[2] D. Gatinel, C. Pagnoulle, Y . Houbrechts, and L. Gobin, “Design and qualification of a diffractive trifocal optical profile for intraocular lenses,” Journal of Cataract & Refractive Surgery, vol. 37, no. 11, pp. 2060–2067, 2011.
[3] R. F. Oliveira, V. Vargas, A. B. Plaza-Puche, and J. L. Alió, “Long-term results of a diffractive trifocal intraocular lens: visual, aberrometric and patient satisfaction results,” European Journal of Ophthalmology, vol. 30, no. 1, pp. 201– 208, 2020.
[4] B. Singh, S. Sharma, S. Dadia, N. Bharti, and S. Bharti, “Comparative evaluation of visual outcomes after bilateral implantation of a diffractive trifocal intraocular lens and an extended depth of focus intraocular lens,” Eye and Contact Lens: Science and Clinical Practice, vol. 46, 2019.
[5] F. Poyales, N. Garzón, D. Pizarro, S. Cobreces, and A. Hernández, “Stability and visual outcomes yielded by three intraocular trifocal lenses with same optical zone design but differing material or toricity,” European Journal of Ophthalmology, vol. 29, no.4, pp. 417–425, 2019.
[6] T. B. Ferreira and F. J. Ribeiro, “Prospective comparison of clinical performance and subjective outcomes between two diffractive trifocal intraocular lenses in bilateral cataract surgery,” Journal of Refractive Surgery, vol. 35, no. 7, pp. 418–425, 2019.
[7] I. Ferreira-Ríos, K. Zuñiga-Posselt, J. C. Serna-Ojeda, and E. Chávez-Mondragón, “Objective and subjective results following implantation of the FineVision trifocal intraocular lens in Mexican patients,” International Ophthalmology, vol. 38, no. 6, pp, 2617–2622, 2018.
[8] A. M. de Carneros-Llorente, A. M. de Carneros, P. M. de Carneros-Llorente, and I. Jiménez-Alfaro, “Comparison of visual quality and subjective outcomes among 3 trifocal intraocular lenses and 1 bifocal intraocular lens,” Journal of Cataract & Refractive Surgery, vol. 45, no. 5, pp. 587–594, 2019.
[9] N. Z. Gregori, T. S. Spencer, N. Mamalis, and R. J. Olson, “In vitro comparison of glistening formation among hydrophobic acrylic intraocular lenses,” Journal of Cataract & Refractive Surgery, vol. 28, no. 7, pp. 1262–1268, 2002.
[10] A. Chang and M. Kugelberg, “Posterior capsule opacification 9 years after phacoemulsification with a hydrophobic and a hydrophilic intraocular lens,” European Journal of Ophthalmology, vol. 27, no. 2, pp. 164–168, 2017.
[11] Y. Li, J. Wang, Z. Chen, and X. Tang, “Effect of hydrophobic acrylic versus hydrophilic acrylic intraocular lens on posterior capsule opacification: meta-analysis,” PLoS One, vol. 8, no. 11, Article ID e77864, 2013.
[12] Z. Z. Nagy, A. Popper-Sachetti, and H. J. Kiss, “Comparison of visual and refractive outcomes between hydrophilic and hydrophobic trifocal intraocular lenses sharing the same optical design,” Journal of Cataract & Refractive Surgery, vol. 45, no. 5, pp. 553–561, 2019.
[13] B. Cochener, J. Vryghem, P. Rozot et al., “Clinical outcomes with a trifocal intraocular lens: a multicenter study,” Journal of Refractive Surgery, vol. 30, no. 11, pp. 762–768, 2014.
[14] B. Cochener, J. Vryghem, and P. Rozot, “Visual and refractive outcomes after implantation of a fully diffractive trifocal lens,” Clinical Ophthalmology, vol. 6, pp. 1421–1427, 2012.
[15] J. C. Vryghem and S. Heireman, “Visual performance after the implantation of a new trifocal intraocular lens,” Clinical Ophthalmology, vol. 7, pp. 1957–1965, 2013.
[16] R. Bilbao-Calabuig, A. Llovet-Rausell, J. Ortega-Usobiaga et al., “Visual outcomes following bilateral implantation of two diffractive trifocal intraocular lenses in 10 084 eyes,” American Journal of Ophthalmology, vol. 179, pp. 55–66, 2017.
[17] P. Mojzis, L. Kukuckova, K. Majerova, P. Ziak, and D. P. Piñero, “Postoperative visual performance with a bifocal and trifocal diffractive intraocular lens during a 1-year follow-up,” International Journal of Ophthalmology, vol. 10, pp. 1528– 1533, 2017.
[18] J. L. Alió, R. Montalbán, P. Peña-García, F. A. Soria, and A. Vega-Estrada, “Visual outcomes of a trifocal aspheric diffractive intraocular lens with microincision cataract surgery,” Journal of Refractive Surgery, vol. 29, no. 11, pp. 756–761, 2013.
[19] Z. Shen, Y. Lin, Y. Zhu, X. Liu, J. Yan, and K. Yao, “Clinical comparison of patient outcomes following implantation of trifocal or bifocal intraocular lenses: a systematic review and meta-analysis,” Scientific Reports, vol. 7, no. 1, Article ID 45337, 2017.
[20] X. Liu, L. Xie, and Y. Huang, “Comparison of the visual performance after implantation of bifocal and trifocal intraocular lenses having an identical platform,” Journal of Refractive Surgery, vol. 34, no. 4, pp. 273–280, 2018.
[21] G. Kondylis, O. Klavdianou, and S. Palioura, “Multifocal and extended depth of focus intraocular lenses,” Annals of Eye Science, vol. 4, 2019.
[22] D. Gatinel and J. Loicq, “Clinically relevant optical properties of bifocal, trifocal, and extended depth of focus intraocular lenses,” Journal of Refractive Surgery, vol. 32, no. 4, pp. 273– 280, 2016.
Deja un comentario cancel
Entradas recientes
- KDB GLIDE: El único dispositivo para Goniotomía aprobado por la FDA para retirar la MT y reducir la PIO.
- Goniotomía con Kahook Dual Blade versus inyección de iStent: Resultados a largo plazo en pacientes con glaucoma de ángulo abierto
- Resultados de iStent Inject versus Kahook Dual Blade en pacientes con Glaucoma sometidos a Cirugía de Cataratas
- Seguimiento a un año de un lente intraocular multifocal con optimización de la tecnología de cambio de fase elevada
- Resultados Clínicos del Implante Ahmed ClearPath en Ojos con Glaucoma: Un Novedoso Dispositivo de Drenaje sin Válvula
DIRECCIÓN
Av. Panamericana A 14 Col. Pedregal de Carrasco C.p. 04700 Coyoacán, Ciudad de México.





Pingback: doxycycline mono 100mg cap
Pingback: levitra price
Pingback: doxycycline for uti